In caso di insufficienza cardiaca, la funzione di pompaggio è indebolita e il cuore non è più in grado di fornire all’organismo la quantità sufficiente di sangue e ossigeno. Più l’insufficienza cardiaca è in uno stadio avanzato, minore sarà l’aspettativa di vita del paziente. Determinate sostanze nutritive forniscono energia per le cellule del muscolo cardiaco e possono aiutare a migliorare la funzione di pompaggio del cuore.
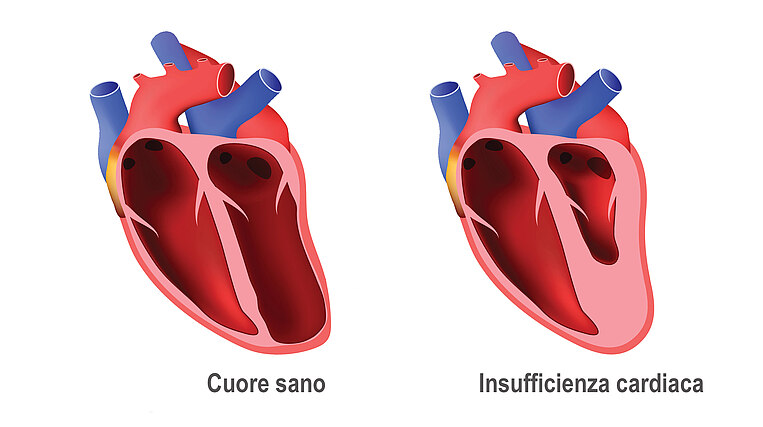
Cause e sintomi
In caso di insufficienza cardiaca il sangue ristagna prima di raggiungere i due ventricoli e non irrora a sufficienza organi e tessuti. Con la progressione della malattia, il liquido si accumula negli organi e può causare formazione di accumuli di acqua nei polmoni, trombosi, aritmie, ictus oppure, nel peggiore dei casi, collasso cardiaco letale.
L’insufficienza cardiaca può colpire la metà sinistra del cuore, quella destra o entrambe. La forma più frequente è l’insufficienza cardiaca sinistra. Il sangue ristagna nella vena polmonare e nella metà sinistra del cuore, dove il sangue ricco di ossigeno viene pompato dal polmone e distribuito nell’organismo. L’insufficienza cardiaca destra colpisce invece la metà destra del cuore, e in questo caso il sangue ristagna nelle vene, quindi nei vasi che trasportano il sangue dagli organi e dai tessuti di nuovo al cuore. Si parla poi di insufficienza cardiaca globale se interessa entrambe le metà del cuore.
Cause: nella maggior parte dei casi l’insufficienza cardiaca è la conseguenza di un’altra patologia che danneggia il muscolo cardiaco o i vasi sanguigni. Una causa frequente è l’infarto cardiaco a seguito di coronaropatia con restringimento delle coronarie a causa dell’arteriosclerosi. Altri importanti fattori di rischio sono l’ipertensione (pressione arteriosa alta), le aritmie come la fibrillazione atriale, le palpitazioni (tachicardia) o la riduzione della frequenza cardiaca (bradicardia).
Sintomi: il grado di gravità è suddiviso in quattro classi (da I a IV) in base alla classificazione della New York Heart Association (NYHA). A seconda della gravità dell’insufficienza cardiaca, il disturbo può rimanere latente oppure danneggiare le capacità fisiche del soggetto. Tra i sintomi di insufficienza cardiaca figurano
- insufficienza respiratoria, debolezza, stanchezza, spossatezza dopo uno sforzo;
- accumuli di liquido (gambe o pancia gonfia, aumento di peso), minzione notturna;
- capogiro, batticuore, collasso circolatorio;
- tosse secca, in particolare di notte;
- perdita di appetito, nausea, sensazione di pienezza, pancia gonfia, stipsi, mal di pancia;
- a volte anche perdita di peso, disturbi della memoria o stato confusionale.
Obiettivi del trattamento
Qual è il trattamento classico dell’insufficienza cardiaca?
Controlli e terapia causale dei fattori di rischio: la terapia ha lo scopo di trattare o controllare i fattori di rischio che spesso accompagnano l’insufficienza cardiaca, come ipertensione, diabete mellito o colesterolo alto. In caso di problemi circolatori dovuti ad arteriosclerosi o cardiopatia coronarica, si ricorre spesso all’inserimento di un bypass per rifornire di nuovo al cuore il sangue sufficiente.
Farmaci: prima di ricorrere all’intervento, i medici tentano di alleviare i sintomi con i farmaci, che possono aiutare il cuore in vari modi:
- Gli ACE inibitori riducono la pressione, ritardano la progressione dell’insufficienza cardiaca e sono i farmaci di prima scelta a partire da un’insufficienza di grado I NYHA poiché migliorano la mortalità e la prognosi. Tra questi figurano: benazepril (Tenkuoren®), ramipril (come Triatec®) o enalapril (come Converten®).
- Gli AT1-antagonisti sono presi in considerazione se un paziente non tollera gli ACE inibitori, ad esempio se soffre di tosse secca come effetto collaterale. Tra questi figurano: candesartan (come Blopress® e Ratacand®) o losartan (come Lortaan®).
- I betabloccanti riducono la frequenza del battito e abbassano la pressione. Sono prescritti in caso di insufficienza cardiaca (NYHA I) a seguito di infarto cardiaco e in caso di insufficienza di classe NYHA II-IV. Tra questi figurano: bisoprololo (come Cardicor® e Congescor®), carvedilolo (come Caravel® e Carvipress®) o metoprololo succinato (come Metoprololo Hexal®).
- I diuretici eliminano l’acqua in eccesso, alleggerendo il cuore. Tra questi figurano: idroclorotiazide (come Esidrex®, Benazepril Isoclorotiazide EG®) e spironolattone (come Aldactone®, Spirolang®).
- I glicosidi cardiaci come i digitalici migliorano la potenza del cuore, riducono le pulsazioni e sono quindi utilizzati in caso di aritmie con la tachicardia. Tra questi figurano: Eudigox® e Lanoxin®.
Se in caso di grave insufficienza cardiaca i sintomi non migliorano, è possibile avviare una speciale terapia di resincronizzazione cardiaca che stimola l’attività dei due ventricoli. In questo caso il paziente deve sottoporsi a intervento chirurgico.
Stile di vita: uno stile di vita sano fa la differenza. Perdere peso aiuta ad alleggerire il cuore indebolito. Un controllo regolare del peso contribuisce a rilevare prematuramente un aumento del ristagno di liquidi e il conseguente peggioramento della funzione cardiaca. Le persone colpite da questo aumento di liquidi dovrebbero discutere con il medico qual è la corretta quantità di liquidi per loro. In linea generale, in caso di grave insufficienza cardiaca si consiglia di non bere più di 1,5-2 litri di liquidi al giorno e di evitare pietanze molto salate come insaccati e piatti pronti, perché il sale si lega con l’acqua appesantendo ulteriormente il cuore.
Si dovrebbe anche smettere di fumare e limitare il consumo di alcol. L’attività fisica adatta per l’insufficienza cardiaca, come ad esempio uscire a camminare o iscriversi a un gruppo che pratica sport cardiaci, può essere altrettanto utile.
Gli obiettivi della medicina dei micronutrienti
La terapia basata sui micronutrienti può integrare al meglio il trattamento contro l’insufficienza cardiaca. Vitamine, minerali e altre sostanze nutritive sono importanti per il funzionamento delle cellule del muscolo cardiaco perché migliorano la funzione di pompaggio del cuore e aiutano ad alleviare i disturbi. Inoltre, supportano l’efficacia dei farmaci, contribuendo a ridurre il dosaggio e gli effetti collaterali.
- Il coenzima Q10 e la carnitina aumentano l’apporto di energia nel muscolo cardiaco.
- Gli acidi grassi omega-3 migliorano i marcatori di rischio e riducono le infiammazioni.
- Il magnesio regola la pressione sanguigna.
- Le vitamine del gruppo B riducono l’omocisteina, un altro fattore di rischio.
I farmaci per il cuore possono inoltre causare carenze, compensate dai micronutrienti adatti.
Trattamento con i micronutrienti
Il coenzima Q10 supporta il metabolismo energetico delle cellule del muscolo cardiaco
Meccanismo d’azione del coenzima Q10
Il coenzima Q10 è una sostanza endogena simile alle vitamine. È presente nei mitocondri, le centrali energetiche delle nostre cellule, ed è necessario per la produzione di energia. Il coenzima Q10 ha un effetto ipotensivo e può influire positivamente sulla capacità di contrazione del muscolo cardiaco. È anche un antiossidante e può quindi evitare ulteriori danni ai vasi.
Studi condotti negli USA e in Europa hanno mostrato che il coenzima Q10 è una soluzione terapeutica integrativa per pazienti con insufficienza cardiaca cronica. Nello studio Q-SYMBIO sono stati arruolati 420 pazienti con insufficienza cardiaca cronica. Nei pazienti che hanno assunto 100 milligrammi di coenzima Q10 tre volte al giorno in aggiunta alla terapia convenzionale, ha avuto luogo un miglioramento della gittata cardiaca e una riduzione di quasi il 50% del rischio di morte cardiaca rispetto ai pazienti trattati con un placebo. Sono necessari ulteriori studi a conferma dei risultati.
Informazioni
Con l’avanzare dell’età l’organismo è in grado di produrre quantità sempre inferiori di coenzima Q10. All’età di 39-43 anni, la produzione di coenzima Q10 è già ridotta di un terzo rispetto ai 20 anni, a tale riduzione supera la metà una volta giunti all’età di 77-81 anni.
Dosaggio e consigli sull’assunzione del coenzima Q10
In caso di cardiopatie e insufficienza cardiaca si consiglia di assumere da 100 a 300 milligrammi di coenzima Q10 al giorno. Nella maggior parte degli studi i soggetti hanno ricevuto il coenzima Q10 per un periodo di tre mesi, con un periodo massimo di somministrazione di due anni. Ecco perché si consiglia di assumerlo per lunghi periodi.
Il coenzima Q10 è liposolubile, pertanto è preferibile prenderlo insieme ad un pasto.
Nonostante sia generalmente ben tollerato, in rari casi può causare lievi disturbi gastrointestinali ed eruzioni cutanee.
Da considerare in caso di malattie e assunzione di farmaci
Le persone con pressione bassa o che assumono farmaci per regolare la pressione dovrebbero, per sicurezza, discutere prima con il proprio medico l’eventuale assunzione di coenzima Q10, perché ha un effetto antipertensivo. Anche i diabetici dovrebbero tenere sempre presenti gli effetti del coenzima Q10, perché può abbassare la glicemia.
Inoltre, riduce l’efficacia degli anticoagulanti cumarinici, che includono i principi attivi fenprocumone e warfarin (Coumadin®). Il suo effetto è stato osservato già a dosi da 30 a 100 milligrammi al giorno. La somministrazione va quindi valutata con il proprio medico, che controllerà il tempo di protrombina (tempo di Quick) e, eventualmente, adeguerà la dose.
L’L-carnitina migliora le prestazioni del muscolo cardiaco
Meccanismo d’azione dell’L-carnitina
L’L-carnitina è una delle sostanze simili alle vitamine e viene prodotta nel fegato e nei reni dagli aminoacidi L-lisina e L-metionina. Può anche essere assunta tramite l’alimentazione. L’L-carnitina ha un ruolo importante nella produzione di energia all’interno dell’organismo poiché è necessaria per trasformare i grassi in energia. Una sua carenza può favorire le aritmie.
Informazioni
Soprattutto i vegetariani e i vegani sono soggetti spesso a una carenza di L-carnitina, contenuta prevalentemente nella carne.
Un’analisi di 17 studi condotti su oltre 1.600 soggetti ha evidenziato che la somministrazione di L-carnitina a pazienti con insufficienza cardiaca cronica allevia i sintomi, migliora le prestazioni del muscolo cardiaco e al contempo riduce il livello di un determinato ormone (Brain Natriuretic Peptide, BNP), che aumenta in caso di insufficienza cardiaca e che serve a controllare la progressione.
Un ulteriore studio ha dimostrato che la somministrazione di L-carnitina per dodici mesi attenua l’ingrossamento del ventricolo sinistro (insufficienza cardiaca sinistra). In caso di ischemia, l’L-carnitina ha ridotto i danni al muscolo cardiaco.
L-carnitina: dosaggio e consigli sull’assunzione
In caso di insufficienza cardiaca si consiglia una dose compresa tra 1.000 e 6.000 milligrammi di L-carnitina al giorno, distribuita in più pasti, ad esempio 1.000 milligrammi due volte al giorno.
Particolarmente efficace è, inoltre, la combinazione di carnitina e coenzima Q10, perché si supportano a vicenda. Secondo uno studio, la somministrazione di 1.200 milligrammi di L-carnitina e di 150 milligrammi di coenzima Q10 al giorno, insieme a un nuovo piano alimentare, può migliorare il benessere fisico e psichico e la prognosi a seguito di infarto cardiaco.
La carnitina è ben tollerabile e solo in singoli casi sono stati riscontrati lievi disturbi gastrointestinali come nausea, vomito, crampi e diarrea.
Da considerare in caso di malattie e assunzione di farmaci
Nei diabetici l’L-carnitina migliora l’indice glicemico. Se si assume L-carnitina contemporaneamente a farmaci ipoglicemizzanti, c’è il rischio di ipoglicemia. Tra questi farmaci figurano la metformina (Metforal®, Metfonorm® e Glucophage®) e le sulfoniluree (Euglucon®, Bi-Euglucon® o Maninil®). Potrebbe eventualmente essere necessario adeguare la dose dei farmaci. Si consiglia di controllare regolarmente l’indice glicemico e di consultare il proprio medico.
In casi molto rari l’L-carnitina può rafforzare l’effetto degli anticoagulanti di tipo cumarinico (antagonisti della vitamina K), tra cui l’etil biscoumacetato (Tromexan®), il fenprocumone (Marcuphen®, Falithrom®, Marcoumar®) e il warfarin (Coumadin®). Pertanto, se si prendono già questi farmaci, l’assunzione di L-carnitina andrebbe discussa con il medico, che controllerà il fattore di coagulazione (valore INR).
Chi soffre di insufficienza renale cronica dovrebbe discutere con il proprio medico l’eventuale assunzione di preparati a base di dosi elevate di L-carnitina (oltre 1.000 milligrammi). Sebbene questi pazienti presentino spesso una carenza di L-carnitina, la sua assunzione a lungo termine da parte di pazienti nefropatici non è supportata da studi sufficienti.
Anche chi ha un tumore dovrebbe discuterne l’assunzione con il proprio medico.
Gli acidi grassi omega-3 arrestano le infiammazioni nei vasi sanguigni
Meccanismo d’azione degli acidi grassi omega-3
Gli acidi grassi omega-3 sono vitali per l’organismo, che non è in grado di produrli autonomamente. Particolarmente importanti sono l’EPA (acido eicosapentaenoico) e il DHA (acido docosaesaenoico), che bloccano le reazioni infiammatorie nei vasi, riducono il livello dei lipidi (solo i trigliceridi) e hanno un effetto antipertensivo poiché dilatano i vasi.
Una protezione contro gli infarti cardiaci: studi condotti negli Stati Uniti hanno dimostrato che gli acidi grassi omega-3 riducono il rischio di infarto. Ciò è stato confermato anche da una valutazione di tre studi di alto livello con un totale di 32.000 partecipanti: dai risultati ottenuti è emerso che l’assunzione di acidi grassi omega-3 comprensivi di EPA e DHA riduce la frequenza di eventi cardiovascolari acuti (ad es. infarto) di quasi la metà rispetto ai soggetti partecipanti come controllo.
Miglioramento della funzione di pompaggio: secondo uno studio condotto su oltre 200 soggetti con insufficienza cardiaca sinistra, l’assunzione di 1.000 milligrammi di acidi grassi omega-3 migliora la funzione di pompaggio danneggiata e i marcatori BNP. Il BNP è un ormone che svolge un ruolo importante nel controllo del bilancio idrico e della pressione.
Dosaggio e consigli sull’assunzione degli acidi grassi omega-3
Si consiglia di assumere 1.500-2.500 milligrammi di acidi grassi omega-3 al giorno con un’elevata percentuale di EPA, perché l’EPA ha un forte effetto antinfiammatorio.
Gli acidi grassi omega-3 andrebbero assunti durante i pasti. I preparati in cui gli acidi grassi omega-3 si presentano nella loro forma di legame naturale come trigliceridi sono utilizzati in modo molto più efficiente dall’organismo rispetto a quelli in cui gli acidi grassi omega-3 sono presenti nella forma etil-estere. Qui sono disponibili consigli sui preparati adatti e sull’assunzione.
Controllo dell’indice omega-3
L’indice omega-3 è ideale per determinare l’apporto di acidi grassi omega-3 nel sangue poiché mostra la loro concentrazione (EPA e DHA) nei globuli rossi (eritrociti). I valori ottimali superano l’otto percento, mentre al di sotto del cinque percento si parla di carenza.
Da considerare in caso di assunzione di anticoagulanti
L’assunzione di dosi elevate di acidi grassi omega-3 (EPA/DHA) può aumentare il rischio di emorragia. Per questo motivo, i pazienti che fanno uso concomitante di anticoagulanti come il warfarin (Coumadin®) e di acidi grassi omega-3 (oltre i 1.000 milligrammi al giorno di EPA/DHA) dovrebbero sottoporsi a regolari controlli medici per verificare i loro valori di coagulazione (tempo di protrombina o INR). Nella sezione relativa al sovradosaggio e alle interazioni sono descritte ulteriori interazioni con gli acidi grassi omega-3.

La vitamina D migliora la frazione di eiezione del cuore
Meccanismo d’azione della vitamina D
L’organismo è in grado di produrre autonomamente la vitamina D, sintetizzata dalla pelle per effetto del sole. I pazienti con insufficienza cardiaca, così come molte persone anziane, soffrono spesso di una carenza di vitamina D. Gli anziani si espongono poco al sole e questo comporta un calo nella produzione di questa vitamina. Le persone con carenza di vitamina D sono più a rischio di collasso cardiaco. Al contrario, un corretto apporto di vitamina D consente di ridurre i livelli dell’infiammazione a carico del sistema cardiocircolatorio.
Uno studio ha dimostrato che l’assunzione di vitamina D per sei mesi migliora sensibilmente la frazione di eiezione del ventricolo sinistro e la conseguente funzione di pompaggio del cuore in pazienti con insufficienza cardiaca cronica. I soggetti in studio hanno ricevuto ogni giorno 4.000 unità internazionali (UI) di vitamina D3 oppure un placebo.
Un piccolo studio clinico ha concluso che l’assunzione di vitamina D migliora le capacità fisiche in un test del cammino in 6 minuti. Dopo l’assunzione di vitamina D per tre mesi, la distanza percorsa dai partecipanti è passata da 210 metri a 225 metri. Un ulteriore studio è giunto a un risultato simile con una somministrazione settimanale di 200.000 unità internazionali di vitamina D3. Contemporaneamente, è diminuito anche il livello di proBNP nel sangue, un importante marcatore per l’insufficienza cardiaca.
Dosaggio e consigli sull’assunzione
In caso di insufficienza cardiaca, si consiglia di assumere ogni giorno da 2.000 a 5.000 unità internazionali di vitamina D, somministrabili anche in dosi settimanali (da 14.000 a 35.000 unità internazionali). L’unico modo per definire la dose corretta è sottoporsi a un controllo del livello di vitamina D nel sangue.
In caso di carenza, è necessario aumentare la dose per un determinato lasso di tempo, ad esempio assumendo ogni giorno 10.000 unità internazionali di vitamina D. Come regola generale, 10.000 unità internazionali al giorno, in aggiunta alla quantità prodotta dall’organismo, consentono di aumentare il livello di vitamina D di 10 nanogrammi per millilitro.
Determinazione dei livelli di vitamina D nel sangue
La vitamina D viene misurata nel siero, la parte liquida del sangue priva di cellule ematiche. Più precisamente, l’esame di laboratorio consente di determinare il livello della sua forma di trasporto, la vitamina D 25(OH), detta anche calcidiolo.
Per gli esperti in micronutrienti il livello di vitamina D dovrebbe essere compreso tra 40 e 60 nanogrammi per millilitro, mentre si parla di carenza se il valore è inferiore a 20 nanogrammi per millilitro.
Da considerare in caso di assunzione di diuretici (tiazidici)
I diuretici tiazidici riducono la quantità di calcio eliminata attraverso i reni, mentre la vitamina D aumenta il livello di questo minerale nel sangue. Di conseguenza, se assunti contemporaneamente, sarebbe necessario sottoporsi a controlli medici regolari per determinare la quantità di calcio presente nel sangue.
Il magnesio normalizza la pressione sanguigna
Meccanismo d’azione
Il magnesio, importante per l’equilibrio elettrolitico e la funzione muscolare, è un antagonista del calcio e ne riduce quindi l’afflusso alle cellule muscolari, rilassando i vasi sanguigni. In questo modo normalizza la pressione sanguigna e protegge i vasi. Un malfunzionamento delle pareti interne dei vasi (endotelio) ha un ruolo critico nella progressione di un’insufficienza cardiaca.
Secondo uno studio, l’assunzione di magnesio per tre mesi migliora la funzione endoteliale, le prestazioni fisiche e la qualità della vita dei pazienti con insufficienza cardiaca sintomatica.
Inoltre, può avere effetti positivi sulle cause più frequenti di insufficienza cardiaca, come arteriosclerosi e aritmie. Contemporaneamente, come dimostrato da alcuni studi, riduce il valore della PCR (proteina C-reattiva), un marcatore importante per le infiammazioni che danneggiano i vasi e per le malattie cardiovascolari, e può quindi migliorare la prognosi in caso di insufficienza cardiaca.
Dosaggio e consigli sull’assunzione
In caso di insufficienza cardiaca, si consiglia di assumere da 300 a 800 milligrammi di magnesio al giorno, preferibilmente sotto forma di magnesio taurato. La taurina stimola infatti la funzione cardiaca. Livelli troppo bassi, ma anche troppo elevati, di magnesio (da 1,50 millimoli per litro di sangue intero) hanno un effetto negativo, soprattutto in pazienti con insufficienza cardiaca. Pertanto, chi assume dosi di magnesio superiori ai 250 milligrammi al giorno dovrebbe sottoporsi a regolari controlli per monitorarne il livello nel sangue.
Per evitare disturbi gastrointestinali come la diarrea, la dose consigliata andrebbe distribuita durante la giornata.
Magnesio: esami di laboratorio
Il magnesio è presente soprattutto nei globuli rossi (eritrociti), quindi gli esami andrebbero condotti sul sangue intero che contiene tutte le cellule ematiche e non solo la componente liquida (siero).
I valori normali del magnesio sono compresi tra 1,38 e 1,50 millimoli per litro di sangue intero, mentre nel siero oscillano da 0,73 a 1,06 millimoli per litro.
Da considerare in caso di assunzione di farmaci e malattie
Il magnesio può ridurre l’efficacia di determinati antibiotici a base di inibitori della DNA girasi e di tetracicline. Può inoltre influenzare l’effetto dei farmaci contro l’osteoporosi (bifosfonati). I pazienti che necessitano di questi farmaci dovrebbero assumere il magnesio rispettando un intervallo di due ore.
In caso di malattie renali non si dovrebbero assumere preparati a base di magnesio, perché i reni sovraccaricati non sono in grado di eliminare correttamente il magnesio in eccesso, che si accumulerebbe nel sangue.
Protezione di base garantita dalle vitamine del gruppo B
Meccanismo d’azione delle vitamine del gruppo B
Le vitamine del gruppo B aiutano l’organismo a eliminare l’omocisteina, un prodotto metabolico che danneggia i vasi e che è correlato a disturbi cardiovascolari quali coronaropatia, infarto e ictus. L’omocisteina è anche un fattore di rischio indipendente per l’insufficienza cardiaca. Uno studio ha dimostrato che livelli elevati di omocisteina possono aumentare il rischio di decesso in soggetti con insufficienza cardiaca.
Le seguenti vitamine B sono particolarmente importanti in caso di insufficienza cardiaca:
Vitamina B1: le persone colpite da insufficienza cardiaca presentano spesso anche una carenza di vitamina B1, come confermato da un’analisi sistematica di 54 studi. Secondo un altro studio, circa un terzo dei pazienti ospedalizzati per insufficienza cardiaca presentava una carenza di vitamina B1. Questa vitamina può aiutare a migliorare i sintomi e la funzione di pompaggio del cuore.
Vitamine B2, B6 e B12 e acido folico: uno studio condotto su 100 pazienti con insufficienza cardiaca ha mostrato che il 27 percento dei soggetti presentava una carenza di vitamina B2 e il 38 percento di vitamina B6, mentre nel gruppo di controllo, composto da pazienti senza insufficienza cardiaca, tali carenze erano riscontrate solo nel due e nel nove percento dei soggetti.
Come indicato da uno studio su circa 400 adulti sani, l’assunzione giornaliera di 400 microgrammi di acido folico, 2 milligrammi di vitamina B6 e 10 microgrammi di vitamina B12 per un periodo di dodici mesi ha ridotto i fattori di rischio per le malattie cardiovascolari, soprattutto nei soggetti con carenza di acido folico.
Dosaggio e consigli sull’assunzione delle vitamine del gruppo B
In caso di insufficienza cardiaca, si consigliano da 100 a 300 milligrammi di vitamina B1 e da 1 a 5 milligrammi di vitamina B2.
Si consigliano invece le seguenti dosi in caso di livelli elevati di omocisteina: da 5 a 15 milligrammi di vitamina B6, da 400 a 600 microgrammi di acido folico e da 250 a 500 microgrammi di vitamina B12.
Determinazione dei livelli di omocisteina
Poiché l’omocisteina danneggia i vasi sanguigni, in caso di insufficienza cardiaca se ne dovrebbero misurare i livelli ematici con regolarità.
L’omocisteina viene misurata nel plasma, la componente liquida del sangue priva di cellule ematiche. I valori normali sono inferiori a 10 micromoli per litro.
Dosaggi in breve
Vitamine | Dosi giornaliere di micronutrienti consigliate in caso di insufficienza cardiaca in milligrammi (mg), microgrammi (µg) o unità internazionali (UI) |
|---|---|
Vitamina B1 | da 100 a 300 milligrammi (mg) |
Vitamina B2 | da 1 a 5 milligrammi |
Vitamina B6 | da 5 a 15 milligrammi |
Acido folico | da 400 a 600 microgrammi (µg) |
Vitamina B12 | da 250 a 500 microgrammi |
Vitamina D | da 2.000 a 5.000 unità internazionali (UI) |
Minerali | |
|---|---|
Magnesio | da 300 a 1.000 milligrammi |
Zinco | da 10 a 20 milligrammi |
Altre sostanze nutritive | |
|---|---|
Acidi grassi omega-3 | da 1.500 a 2.500 milligrammi con una percentuale elevata di EPA |
Coenzima Q10 | da 100 a 300 milligrammi |
L-carnitina | da 1.000 a 6.000 milligrammi |
Esami di laboratorio consigliati in breve
Esami di laboratorio consigliati in caso di insufficienza cardiaca
Valori normali | |
|---|---|
Indice omega-3 (siero) | dall’8 all’11 percento |
Vitamina D | da 40 a 60 nanogrammi per millilitro (ng/ml) |
Magnesio | da 1,38 a 1,50 millimoli per litro (mmol/l) nel sangue intero da 0,73 a 1,06 millimoli per litro nel siero |
Omocisteina | <10 micromoli per litro (µmol/l) |
Sostegno ai farmaci tramite i micronutrienti
Gli ACE inibitori e gli AT1-antagonisti favoriscono la carenza di zinco
L’ipertensione danneggia i vasi e sovraccarica il cuore. Per questo i pazienti con insufficienza cardiaca vengono spesso trattati con farmaci antipertensivi (ACE inibitori) come il captopril (ad esempio Acediur®) o l’enalapril (ad esempio Lanex®, Naprilene®, Converten® o Silverit®). Gli ACE inibitori si legano allo zinco, favorendone così la carenza.
Anche gli AT1-antagonisti come il losartan (Lortaan®) o il candesartan (ad esempio Blopress® e Ratacand®) riducono la pressione. Questi farmaci incrementano in particolare l’eliminazione dello zinco e nel lungo periodo possono causare una carenza.
I medici specializzati in micronutrienti consigliano, parallelamente agli ACE inibitori e agli AT1-antagonisti, anche da 10 a 20 milligrammi di zinco al giorno.
I betabloccanti danneggiano il metabolismo del coenzima Q10
I betabloccanti come il propranololo (ad esempio Hemangiol® o Inderal®) hanno un effetto antipertensivo, ma la loro assunzione può danneggiare il metabolismo del coenzima Q10. Al contrario, quest’ultimo sostiene l’efficacia dei betabloccanti e riduce la pressione.
I medici specializzati in micronutrienti consigliano, come terapia collaterale, di assumere almeno 100 milligrammi di coenzima Q10 al giorno, così da prevenire l’effetto negativo dei betabloccanti sul suo metabolismo.
I diuretici incrementano la perdita di minerali
I diuretici eliminano i liquidi in eccesso. In particolare, i cosiddetti diuretici dell’ansa come il furosemide (ad esempio Diretif®) causano anche la perdita di minerali importanti come magnesio, potassio o zinco e possono ridurre il livello di vitamina B1. I diuretici tiazidici (idroclorotiazide come Benazepril Idroclorotiazide EG®, Esidrex®) favoriscono l’eliminazione di acido folico, vitamina B6 e vitamina B12 e possono aumentare il livello di omocisteina.
Ecco perché i medici specializzati in micronutrienti consigliano di assumere in concomitanza con i diuretici i seguenti nutrienti:
- da 10 a 20 milligrammi di zinco
- da 200 a 400 milligrammi di magnesio
- 40 milligrammi di vitamina B1
- da 5 a 15 milligrammi di vitamina B6
- da 100 a 200 microgrammi di vitamina B12
- da 200 a 400 microgrammi di acido folico
Dosaggi in breve
Dosi giornaliere di micronutrienti consigliate in caso di assunzione di farmaci
ACE inibitori | |
|---|---|
Zinco | da 10 a 20 milligrammi (mg) |
AT1-antagonisti | |
|---|---|
Zinco | da 10 a 20 milligrammi |
Betabloccanti | |
|---|---|
Coenzima Q10 | almeno 100 milligrammi |
Diuretici | |
|---|---|
Acido folico | da 200 a 400 microgrammi (µg) |
Vitamina B1 | 40 milligrammi |
Vitamina B6 | da 5 a 15 milligrammi |
Vitamina B12 | da 100 a 200 microgrammi |
Zinco | da 10 a 20 milligrammi |
Magnesio | da 200 a 400 milligrammi |
Riepilogo
In caso di insufficienza cardiaca, la funzione di pompaggio è indebolita e il cuore non è più in grado di fornire all’organismo la quantità sufficiente di sangue e ossigeno. Determinati micronutrienti possono contribuire ad aumentare l’apporto di energia e migliorare la funzione di pompaggio del cuore, frenando la progressione della malattia.
Il coenzima Q10 supporta il metabolismo energetico del cuore, riduce la pressione e può influenzare positivamente la capacità di contrazione del muscolo cardiaco. L’L-carnitina incrementa le prestazioni del muscolo cardiaco e può alleviare i sintomi dell’insufficienza cardiaca cronica. Gli acidi grassi omega-3 come il DHA e l’EPA inibiscono i processi infiammatori nei vasi, riducono i valori dei lipidi ematici oltre la norma e contribuiscono ad abbassare la pressione sanguigna grazie alla loro azione vasodilatatrice. La vitamina D migliora la frazione di eiezione del cuore e le prestazioni fisiche. Il magnesio riporta la pressione a valori normali e protegge i vasi. Le vitamine del gruppo B riducono l’omocisteina e, quindi, i danni ai vasi, potendo così migliorare la prognosi.
Diversi farmaci per l’insufficienza cardiaca possono avere effetti collaterali, come la perdita di minerali dovuta all’assunzione di ACE inibitori e diuretici, oppure danneggiare il metabolismo del coenzima Q10 causato dai betabloccanti. I micronutrienti come lo zinco, il coenzima Q10, il magnesio e le vitamine del gruppo B possono aiutare a contrastare l’insorgenza di tali effetti collaterali.
Indice degli studi e delle fonti
Ahmed, M. et al. (2015): Thiamin deficiency and heart failure: the current knowledge and gaps in literature. Heart Fail Rev. 2015 Jan;20(1):1-11. https://www.ncbi.nlm.nih.gov/pubmed/24811895, consultato il: 24.01.2018.
Almoznino-Sarafian, D. et al (2007): Magnesium and C-reactive protein in heart failure: an anti-inflammatory effect of magnesium administration? Eur J Nutr. 2007 Jun;46(4):230-7. https://www.ncbi.nlm.nih.gov/pubmed/17479208, consultato il: 23.01.2018.
Angkananard, T. et al. (2016): The association of serum magnesium and mortality outcomes in heart failure patients. Medicine (Baltimore). 2016 Dec; 95(50): e5406. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5268025/, consultato il: 23.01.2018.
Babar, M.Z.M. et al. (2016): Effects of Vitamin D supplementation on physical activity of patients with Heart Failure. Pak J Med Sci. 2016 Nov-Dec; 32(6): 1430–1433. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5216295/, consultato il: 23.01.2018.
Berman, M. et al. (2004): Coenzyme Q10 in patients with end-stage heart failure awaiting cardiac transplantation: a randomized, placebo-controlled study. Clin Cardiol. 2004 May;27(5):295-9. https://www.ncbi.nlm.nih.gov/pubmed/15188947, consultato il: 20.12.2017.
Bundesärztekammer (BÄK), Kassenärztliche Bundesvereinigung (KBV), Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften (AWMF) (2017): Nationale VersorgungsLeitlinie Chronische Herzinsuffizienz – Langfassung, 2. Auflage. 2/2017. http://www.leitlinien.de/mdb/downloads/nvl/herzinsuffizienz/herzinsuffizienz-2aufl-vers2-llr.pdf, consultato il: 20.12.2017.
Cicero, A.F.G. & Colletti, A. (2017): Nutraceuticals and Dietary Supplements to Improve Quality of Life and Outcomes in Heart Failure Patients. Curr Pharm Des. 2017;23(8):1265-1272. https://www.ncbi.nlm.nih.gov/pubmed/28120718, consultato il: 20.12.2017.
Dalbeni, A. et al. (2014): Effects of six months of vitamin D supplementation in patients with heart failure: a randomized double-blind controlled trial. Nutr Metab Cardiovasc Dis. 2014 Aug;24(8):861-8. https://www.ncbi.nlm.nih.gov/pubmed/24787908, consultato il: 23.01.2018.
Deutsche Gesellschaft für Kardiologie – Herz-und Kreislaufforschung e.V. (2017): ESC Pocket Guidelines. Herzinsuffizienz, Version 2016. http://leitlinien.dgk.org/files/PLL_2017_HI_Auflage2.pdf, consultato il: 20.12.2017.
Flanagan, J.L. et al. (2010): Role of carnitine in disease. Nutr Metab (Lond). 2010; 7: 30. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2861661/, consultato il: 21.12.2017.
Fotino, A.D. et al. (2013): Effect of coenzyme Q₁₀ supplementation on heart failure: a meta-analysis. Am J Clin Nutr. 2013 Feb;97(2):268-75. https://www.ncbi.nlm.nih.gov/pubmed/23221577, consultato il: 20.12.2017.
Fuentes, J.C. et al. (2006): Acute and Chronic Oral Magnesium Supplementation: Effects on Endothelial Function, Exercise Capacity, and Quality of Life in Patients With Symptomatic Heart Failure. Congestive Heart Failure, 2006 Jan; 12: 9–13. http://onlinelibrary.wiley.com/doi/10.1111/j.1527-5299.2006.04692.x/full, consultato il: 23.01.2018.
Glück, T. & Alter, P. (2016): Marine omega-3 highly unsaturated fatty acids: From mechanisms to clinical implications in heart failure and arrhythmias. Vascul Pharmacol. 2016 Jul;82:11-9. https://www.ncbi.nlm.nih.gov/pubmed/27080538, consultato il: 21.12.2017.
Gröber, U. (2015): Interaktionen – Arzneimittel und Mikronährstoffe. 2. Aufl. Wissenschaftliche Verlagsgesellschaft mbH Stuttgart.
Gröber, U. (2007): Arzneimittel und Mikronährstoffe, Medikationsorientierte Supplementierung. 1. Aufl. Wissenschaftliche Verlagsgesellschaft mbH Stuttgart.
Jain, A. et al. (2015): Determining the Role of Thiamine Deficiency in Systolic Heart Failure: A Meta-Analysis and Systematic Review. J Card Fail. 2015 Dec;21(12):1000-7. https://www.ncbi.nlm.nih.gov/pubmed/26497757, consultato il: 24.01.2018.
Johansson, P. et al. (2016): Fluid restriction in patients with heart failure: how should we think? Eur J Cardiovasc Nurs. 2016 Aug;15(5):301-4. https://www.ncbi.nlm.nih.gov/pubmed/27169459, consultato il: 14.12.2017.
Katta, N. et al. (2016): Does Long-Term Furosemide Therapy Cause Thiamine Deficiency in Patients with Heart Failure? A Focused Review. Am J Med. 2016 Jul;129(7):753.e7-753.e11. https://www.ncbi.nlm.nih.gov/pubmed/26899752, consultato il: 24.01.2018.
Keith, M.E. et al. (2009): B-vitamin deficiency in hospitalized patients with heart failure. J Am Diet Assoc. 2009 Aug;109(8):1406-10. https://www.ncbi.nlm.nih.gov/pubmed/19631047, consultato il: 24.01.2018.
Luo, T. et al. (2013): A study on the efficacy and safety assessment of propionyl-L-carnitine tablets in treatment of intermittent claudication. Thromb Res. 2013 Oct;132(4):427-32. https://www.ncbi.nlm.nih.gov/pubmed/23998557, consultato il: 21.12.2017.
Mortensen, S.A. et al. (2014): The effect of coenzyme Q10 on morbidity and mortality in chronic heart failure: results from Q-SYMBIO: a randomized double-blind trial. JACC Heart Fail. 2014 Dec;2(6):641-9. https://www.ncbi.nlm.nih.gov/pubmed/25282031, consultato il: 20.12.2017.
Oeing C.U. et al. (2016): The new ESC Guidelines for acute and chronic heart failure. Herz. 2016 Dec;41(8):655-663. https://www.ncbi.nlm.nih.gov/pubmed/27858115, consultato il: 20.12.2017.
Oleck, S. & Ventura, H. (2016): Coenzyme Q10 and Utility in Heart Failure: Just Another Supplement? Curr Heart Fail Rep. 2016 Aug;13(4):190-5. https://www.ncbi.nlm.nih.gov/pubmed/27333901, consultato il: 20.12.2017.
Serban, M.C. et al. (2016): Impact of L-carnitine on plasma lipoprotein(a) concentrations: A systematic review and meta-analysis of randomized controlled trials. Sci Rep. 2016; 6: 19188. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4709689, consultato il: 21.12.2017.
Sharifi, M.A. (2017): Effects of a therapeutic lifestyle change diet and supplementation with Q10 plus L-carnitine on quality of life in patients with myocardial infarction: A randomized clinical trial. J J Cardiovasc Thorac Res. 2017;9(1):21-28. https://www.ncbi.nlm.nih.gov/pubmed/28451084, consultato il: 21.12.2017.
Sharma, A. et al. (2016): Coenzyme Q10 and Heart Failure: A State-of-the-Art Review. Circ Heart Fail. 2016 Apr;9(4):e002639. https://www.ncbi.nlm.nih.gov/pubmed/27012265, consultato il: 20.12.2017.
Singh, R.B. et al. (1996): A randomised, double-blind, placebo-controlled trial of L-carnitine in suspected acute myocardial infarction. Postgrad Med J. 1996 Jan; 72(843): 45–50. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2398308/, consultato il: 21.12.2017.
Song, X. et al. (2017): Efficacy and Safety of L-Carnitine Treatment for Chronic Heart Failure: A Meta-Analysis of Randomized Controlled Trials. Biomed Res Int. 2017;2017:6274854. https://www.ncbi.nlm.nih.gov/pubmed/28497060, consultato il: 21.12.2017.
Trasobares, E. et al. (2007): Effects of angiotensin-converting enzyme inhibitors (ACE i) on zinc metabolism in patients with heart failure. J Trace Elem Med Biol. 2007;21 Suppl 1:53-5. https://www.ncbi.nlm.nih.gov/pubmed/18039498, consultato il: 24.01.2018.
Turrini, F. et al. (2017): Effects of Cholecalciferol Supplementation in Patients with stable heart failure and Low Vitamin D levels (ECSPLOIT-D): a double-blind, randomized, placebo-controlled pilot study. Minerva Cardioangiol. 2017 Dec;65(6):553-562. https://www.ncbi.nlm.nih.gov/pubmed/28565886, consultato il: 23.01.2018.
van der Waal, H.H. et al. (2015): Vitamin B12 and folate deficiency in chronic heart failure. Heart. 2015 Feb;101(4):302-10. https://www.ncbi.nlm.nih.gov/pubmed/25324534, consultato il: 24.01.2018.
Vizzardi, E. et al. (2009): Homocysteine and heart failure: an overview. Recent Pat Cardiovasc Drug Discov. 2009 Jan;4(1):15-21. https://www.ncbi.nlm.nih.gov/pubmed/19149701, consultato il: 24.01.1018.
Watanabe, S. et al. (2016): Associations With Eicosapentaenoic Acid to Arachidonic Acid Ratio and Mortality in Hospitalized Heart Failure Patients. J Card Fail. 2016 Dec;22(12):962-969. https://www.ncbi.nlm.nih.gov/pubmed/27138463, consultato il: 21.12.2017.
Wei, M.Y. & Jacobson, T.A. (2011): Effects of eicosapentaenoic acid versus docosahexaenoic acid on serum lipids: a systematic review and meta-analysis. Curr Atheroscler Rep. 2011 Dec;13(6):474-83. https://www.ncbi.nlm.nih.gov/pubmed/21975919/, consultato il: 27.02.2018.
Wong, A.P. (2016): Myocardial energetics and the role of micronutrients in heart failure: a critical review. Am J Cardiovasc Dis. 2016; 6(3): 81–92. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5030388/, consultato il: 20.12.2017.




