Eine chronisch latente Übersäuerung zählt zu den häufigen Störungen im Säure-Basen-Haushalt. Die dadurch ausgelösten Veränderungen im Stoffwechsel können die Nieren auf verschiedenen Wegen schädigen, deren Filterfunktion im Alter ohnehin nachlässt. Damit kann weniger Säure aus dem Körper ausgeschieden werden – und das Risiko für eine Azidose steigt. Eine erhöhte Säurebelastung des Körpers steigert zudem das Risiko für Nierensteine.
Eine basische Ernährung, die viel Obst und Gemüse enthält, kann einer Übersäuerung entgegenwirken. Unterstützung können Basenpräparate bieten: Sie versorgen uns mit wichtigen Mineralstoffen wie Calcium, Kalium und Magnesium sowie mit Citrat, aus dem der Körper Bicarbonat – die wichtigste Puffersubstanz im Blut – bilden kann.
Die Rolle der Nieren im Säure-Basen-Haushalt
Die beiden Nieren spielen eine sehr wichtige Rolle bei dem Prozess, das Gleichgewicht des Säure-Basen-Haushalts im Körper aufrechtzuerhalten. Denn sie können als einziges Organ Säuren in relevanten Mengen direkt ausscheiden. Das ist insbesondere für die sogenannten nicht flüchtigen Säuren entscheidend – und wenn eine Übersäuerung vorliegt.
Nicht flüchtige Säuren beziehungsweise ihre Anionen stammen aus Nahrungsproteinen und bestimmten Pflanzen sowie aus Fertigprodukten. Dabei handelt es sich vorwiegend um:
- Schwefelsäure (Sulfat): Sie entsteht größtenteils bei der Verstoffwechselung von Lebensmitteln, die schwefelhaltige Aminosäuren wie Cystein enthalten. Dazu gehören insbesondere tierische Produkte (Fleisch, Fisch, Käse, Eier) und auch Hülsenfrüchte wie Soja sowie Getreide.
- Phosphorsäure (Phosphat): Sie steckt sowohl in eiweißhaltigen Nahrungsmitteln als auch in Fertigprodukten, denen Phosphate zugesetzt wurden – wie zum Beispiel Schmelzkäse oder Cola.
- Oxalsäure (Oxalat): Sie wird über pflanzliche Lebensmittel wie Rhabarber, Spinat oder Rote Bete zugeführt.
Nahrungsmittel, die diese Säuren beziehungsweise Säurevorstufen enthalten, werden als säurebildend bezeichnet. Nicht flüchtige Säuren beziehungsweise einen Protonenüberschuss müssen die Nieren ausscheiden, um das Säure-Base-Gleichgewicht aufrechtzuerhalten.
Organische Säuren wichtig für Bicarbonat-Bildung
Dagegen wirken organische Säuren beziehungsweise ihre Salze – wie insbesondere Citronensäure und Citrat, aber auch Äpfelsäure und Malat – aus pflanzlichen Lebensmitteln basisch: Sie werden im Darm resorbiert und führen zur Bildung von Bicarbonat. Dieses dient im Blut als wertvolle Puffersubstanz, und kann überschüssige Wasserstoff-Ionen (Protonen, H+) aufnehmen. Dabei entsteht Kohlensäure (H2CO3), die als flüchtige Säure bezeichnet wird. Denn sie zerfällt in Kohlendioxid (CO2), das über die Lungen abgeatmet wird, und Wasser (H2O).
Aus der Differenz zwischen den im Körper (endogen) produzierten beziehungsweise den aufgenommenen nicht flüchtigen Säuren und den resorbierten Alkalivorstufen ergibt sich die Säurebelastung durch die Nahrung. Diese wird auch als endogene Nettosäureproduktion (englisch: net endogenous acid production (NEAP)) bezeichnet.
Für den Körper und seine Stoffwechselaktivität ist ein ausgeglichener Säure-Basen-Haushalt wichtig. Deshalb regeln die Nieren die systemische Bicarbonat-Konzentration auf zwei Wegen:
- Sie resorbieren im Normalfall das wichtige Bicarbonat fast vollständig zurück.
- Zudem bilden sie neues Bicarbonat, um die verbrauchte Puffersubstanz zu ersetzen.
Laborwert für den Bicarbonat-Spiegel
Mit der Blutgasanalyse – aus arteriellem beziehungsweise Kapillarblut – lässt sich der Wert für Bicarbonat (Standard-Bicarbonat) bestimmen. Sowohl für Frauen als auch für Männer liegt der Referenzwert bei
- 22–26 Millimol pro Liter (mmol/l) (international standardisierte Angabe) oder
22–26 Milliequivalente pro Liter (mEq/l).
Weicht der Bicarbonat-Wert im Blut davon ab, weist dies auf einen gestörten Säure-Basen-Haushalt hin:
- < 22 mmol/l: metabolische Azidose
- > 26 mmol/l: metabolische Alkalose
Die Nieren enthalten jeweils ungefähr eine Million kleiner Funktionseinheiten, die Nephrone. Ein Nephron setzt sich aus dem Nierenkörperchen und einem angeschlossenem Nierenröhrchen (Nierentubulus) zusammen. Das Nierenkörperchen wiederum besteht aus dem Glomerulus, einem Knäuel aus Blutkapillaren, das von der schützenden Bowman-Kapsel umgeben ist.
Im Glomerulus werden aus dem Blut Wasser und gelöste Substanzen (passiv) filtriert – es entsteht der sogenannte Primärharn. Im Verlauf der Nierenröhrchen erfolgt eine aktive Rückresorption zahlreicher Stoffe wie zum Beispiel Glucose und der größte Teil des Wassers. Weitere Substanzen wie beispielsweise Ammoniak werden im Tubulussystem aktiv ausgeschieden – es entsteht der Endharn.
In der Niere werden zwei Bereiche unterschieden:
- Nierenrinde: Hier liegen die Nierenkörperchen und die gewundenen Anteile der Nierenröhrchen (Nierentubuli).
- Nierenmark: Hier finden sich die geraden Anteile der Nierentubuli und die feinen Sammelrohre, in denen der Harn über die Nierenkelche und das Nierenbecken (zentraler Sammeltrichter der Niere) bis in die Harnleiter transportiert wird.
Die beiden Harnleiter münden in der Harnblase.
Gut funktionierende Nieren sind lebenswichtig
Unsere beiden Nieren erfüllen viele essenzielle Funktionen:
- Ausscheidung (stickstoffhaltiger) Abfallprodukte,
- Regulation des Elektrolyt-Haushalts,
- Regulierung des Säure-Basen-Haushalts,
- Blutdruckkontrolle,
- Rückresorption lebenswichtiger Substanzen und
- Produktion von Hormonen: Renin zur Blutdruckkontrolle, Erythropoietin, welches die Bildung roter Blutkörperchen anregt, und Calcitriol, die aktivierte Form von Vitamin D.
Die Filterleistung der Nieren ist beachtlich: Etwa 1800 Liter Blut pro Tag werden filtriert. Das bedeutet, dass die gesamte Blutmenge eines Menschen täglich bis zu 300-mal die Nieren durchfließt. Daraus ergeben sich etwa 180 Liter Primärharn, von dem der größte Teil zurückgewonnen wird. Ausgeschieden als Urin werden nur etwa 1,5 Liter.
Beurteilung der Nierenfunktion
Um die Nierenfunktion eines Menschen zu beurteilen, wird die sogenannte glomeruläre Filtrationsrate (GFR) herangezogen. Sie gibt an, wie viel Blutvolumen die Nieren pro Minute filtern – gemessen in Milliliter pro Minute (ml/min). Meist wird sie mithilfe von Kreatininwerten im Blut sowie Alter, Geschlecht und Gewicht geschätzt (eGFR, e für „estimated“).
Mit dem Alter – ab ungefähr 30-35 Jahren beginnend – nimmt die GFR ab; pro Jahr etwa um 0,7–1,0 Prozent.
Alter [Jahre] | Mittlere GFR |
20–29 | 116 ml/min |
30–39 | 107 ml/min |
40–49 | 99 ml/min |
50–59 | 93 ml/min |
60–69 | 85 ml/min |
> 70 | 75 ml/min |
Quelle: https://flexikon.doccheck.com/de/Glomerul%C3%A4re_Filtrationsrate
Eine niedrige GFR oder eGFR kann auf eine Nierenerkrankung hinweisen.
Was beeinträchtigt die Nierenfunktion?
Die Nierenfunktion sinkt mit den Jahren, das bedeutet die glomeruläre Filtrationsrate nimmt ab. Eine Studie untersuchte die Netto-Säureausscheidungskapazität (Net Acid Excretion Capacity (NAEC)) der Nieren in Abhängigkeit vom Alter. Das Ergebnis: Bei Kindern, Jugendlichen und jungen Erwachsenen unterscheidet sich die Fähigkeit, Säure auszuscheiden, nicht wesentlich. Allerdings geht sie bei älteren Menschen (55–75 Jahre) deutlich zurück. Die Autoren schlussfolgern, dass Ältere möglicherweise eine höhere tägliche Zufuhr an alkalisierenden Mineralstoffen benötigen, um den Verlust der Nierenfunktion auszugleichen.
Unterschiedliche Faktoren können zusätzlich die Niere schädigen und zu einer chronischen Nierenschwäche (Niereninsuffizienz) führen. Dazu zählen vor allem Bluthochdruck und die Zuckerkrankheit (Diabetes mellitus): Hoher Blutdruck und hohe Zuckerwerte führen zu krankhaften Veränderungen an den Blutgefäßen. Besonders betroffen sind hiervon die feinen Gefäße, die Kapillaren. Ist der Druck in den feinen Kapillargefäßen der Nieren zu hoch, wird Nierengewebe geschädigt und die Filterleistung der Nieren sinkt.
Im Gegenzug erhöht sich der Blutdruck:
- Geschädigte Nieren können weniger Wasser ausscheiden. Das höhere Blutvolumen steigert den Blutdruck.
- Zudem setzen die erkrankten Nieren mehr blutdrucksteigernde Hormone (Aldosteron) frei.
Ein hoher Blutdruck kann also sowohl Ursache als auch Folge einer chronischen Nierenschwäche sein.
Zudem sind das metabolische Syndrom – das durch Bluthochdruck, Übergewicht sowie durch erhöhten Blutzucker und einen gestörten Fettstoffwechsel geprägt ist – und seine Komponenten mit einem erhöhten Risiko für chronische Nierenerkrankungen verbunden, wie eine aktuelle Studie mit mehr als 450.000 Teilnehmenden gezeigt hat. Diese schloss auch Werte für Harnsäure (als fünften Faktor) ein. Insbesondere, wenn vier oder fünf Faktoren des metabolischen Symptoms auftraten, war die Wahrscheinlichkeit für eine Nierenschwäche deutlich erhöht.
Chronische Nierenerkrankung im Alter verbreitet

Ist die Filterleistung der Nieren dauerhaft beeinträchtigt, sprechen Fachleute von einer chronischen Nierenerkrankung („chronic kidney disease“ (CKD)). In Deutschland sind etwa 9 Millionen Menschen – vor allem über 60-Jährige – von dieser chronischen Nierenschwäche betroffen, wobei die Dunkelziffer vermutlich höher liegt. Denn erste Anzeichen treten oft erst spät auf. Weltweit sind es laut Deutschem Ärzteblatt fast 800 Millionen Menschen, die mit einer verminderten Nierenfunktion leben müssen.
Stadien der chronischen Nierenschwäche (Niereninsuffizienz)
- G1: Normale oder erhöhte GFR (≥ 90 ml/min), mit Anzeichen einer Nierenerkrankung (Eiweiß im Urin).
- G2: Leichte Einschränkung der Nierenfunktion (GFR 60–89 ml/min); Kreatinin (Abbauprodukt des Kreatins) im Blut steigt, oft auch der Blutdruck.
- G3a: Mäßige Einschränkung (GFR 45–59 ml/min); Kreatinin- und Harnstoff-Wert erhöht; beginnende Blutarmut; Phosphat im Blut steigt; weniger aktives Vitamin D im Blut führt zu einem Calciummangel; in der Folge erhöht sich die Menge an Parathormon, was zu einer Calciummobilisierung aus den Knochen und damit zu einer Knochenentkalkung führt.
- G3b: Stärkere Einschränkung (GFR 30–44 ml/min).
- G4: Schwere Einschränkung der Nierenfunktion (GFR 15–29 ml/min); weniger Urin; die Regulation des Säure-Basen-Haushalts versagt, was zu einer Azidose und zum Abbau von Muskeleiweiß (um Puffersubstanzen zu gewinnen) führt.
- G5: Nierenversagen (terminale Niereninsuffizienz) (GFR < 15 ml/min) bedeutet Dialyse- oder Transplantationspflichtigkeit.
GFR = Glomeruläre Filtrationsrate
Die Stadien G1 und G2 werden meist nur zufällig entdeckt. Wenn Symptome vorliegen, besteht mindestens Stadium G3.
(Quelle: https://www.uniklinikum-leipzig.de/einrichtungen/medizinische-klinik-3/Seiten/einteilung.aspx)
Häufigste Gründe für ein Nierenversagen:
- Diabetes (30–40 Prozent)
- schlecht eingestellter Bluthochdruck (25 Prozent)
Eine latente Übersäuerung beeinträchtigt ebenfalls die Nierenfunktion (siehe unten).
Liegt eine chronische Nierenerkrankung (CKD) vor, wird das Renin-Angiotensin-Aldosteron-System (RAAS), welches der Blutdruckregelung dient, übermäßig aktiviert. Das dadurch verstärkt ausgeschüttete Angiotensin II
- sorgt einerseits für einen erhöhten Blutdruck. Dieser führt zu Eiweiß im Urin (Proteinurie) und lässt die Nierenschädigung weiter fortschreiten.
- Zum anderen setzt es schädigende Signalwege in Gang: Die Folgen sind Entzündungen und der Umbau des Nierengewebes zu funktionslosem Bindegewebe (Fibrose). Dadurch sinkt die Filterleistung (GFR) weiter.
Wie führt eine säurelastige Ernährung zu Nierenschäden?
Zum einen kann eine säurelastige Ernährung einen Bluthochdruck bewirken, der die Nierenfunktion beeinträchtigt. Zum anderen kann es zu direkten schädigenden Prozessen in den Nieren kommen:
- Um Stickstoff aus dem Körper zu entfernen, setzt die Leber Ammoniak (NH3) im sogenannten Harnstoffzyklus zu Harnstoff um. Dieser Prozess verbraucht Bicarbonat (HCO3–).
- Besteht ein Säureüberschuss (azidotische Stoffwechsellage) im Körper – auch schon bei einer chronisch latenten Azidose – werden Puffersubstanzen verbraucht – und das Bicarbonat im Blut ist erniedrigt. Das bremst den Harnstoffzyklus und damit auch das verantwortliche Enzym in der Leber, die Glutaminase, die das Ammonium aus Glutamin gewinnt. Stattdessen wird vermehrt Ammonium zusammen mit Glutamat zu Glutamin umgesetzt.
- Im Gegenzug steigt die Aktivität der Glutaminase in den Nieren – in der Folge entsteht dort vermehrt Ammoniak (Ammoniummechanismus). Dieses kann ein Proton (H+) aufnehmen und wird als Ammonium (NH4+) über den Urin aus dem Körper entfernt.
Etwa die Hälfte bis zwei Drittel der netto ausgeschiedenen Säure entfallen auf die NH₄⁺ -Ausscheidung im Urin. - Wenn die Niere Glutamin spaltet, entsteht neben Ammoniak auch Glutamat, welches weiter zu Bicarbonat verstoffwechselt wird. Das bedeutet, dieser Mechanismus produziert Bicarbonat.
Für die renale Protonenausscheidung ist Ammoniak notwendig. Allerdings schädigt die erhöhte Konzentration des giftigen Ammoniaks die Nierenkanälchen (Nierentubuli), die röhrenförmigen Strukturen der Niere. In ihnen werden wichtige Stoffe wie Wasser, Elektrolyte und Nährstoffe zurück ins Blut resorbiert und Abfallprodukte in den Urin ausgeschieden.
Dieser schädigende Prozess scheint vor allem bei bereits beeinträchtigter Nierenfunktion entscheidend zu sein. Denn obwohl die endogene Säureproduktion unverändert blieb, nahm die Fähigkeit, Ammoniak auszuscheiden, mit sinkender glomerulärer Filtrationsleistung ab, wie eine Studie gezeigt hat. Damit einher ging eine höhere Wahrscheinlichkeit für einen schnellen Abfall der Filtrationsleistung und ein signifikant erhöhtes Risiko für terminales Nierenversagen.
Übersäuerung führt zur Rückhaltung von Säure
Wenn sich Menschen säurelastig ernähren, scheiden sie auch vermehrt Säuren aus, wie der deutlich saurere Urin belegt. Eine erhöhte Säurebelastung durch die Ernährung (dietary acid load (DAL)) verstärkt also die Netto-Säureausscheidung (NAE).
Allerdings haben Forschende ermittelt, dass dann weniger Protonen ausgeschieden werden als aufgenommen. Da das Blut seinen pH-Wert nicht ändert, bedeutet dies, dass ein Teil der Protonen ins Körpergewebe gelangt, um dort abgepuffert zu werden. Fachleute sprechen von einer Säure-Retention, einer Rückhaltung von Säure.
Diese Säureretention betrifft auch Patienten und Patientinnen mit chronischer Nierenschwäche, die viele säurebildende Lebensmittel verzehren – selbst ohne ausgeprägte metabolische Azidose. Auch sie scheiden also weniger Säure aus, als sie aufnehmen beziehungsweise produzieren. Gleichzeitig kann die erhöhte Säurebelastung zu einer stärkeren Nierenschädigung führen: Höhere NAE-Werte hängen mit Eiweiß im Urin (Albuminurie) – ein Zeichen für eine Nierenschädigung – und niedriger Filtrationsleistung der Nieren (eGFR) zusammen.
Der Mechanismus dahinter: Die Säureretention bei geminderter Filtrationsleistung erhöht die Spiegel von Aldosteron und Endothelin-1, einem sogenannten Peptidhormon. Durch die Überaktivität von Endothelin kommt es zu einer deutlichen Gefäßverengung (Vasokonstriktion) und in der Folge fällt die glomeruläre Filtrationsleistung ab. Sind bereits Nephrone geschädigt, muss pro Nephron mehr Säure ausgeschieden werden. Dies bewirkt weitere Nierenschäden. Erhöhte Endothelin-1-Spiegel können zudem Entzündungen und Fibrose auslösen, was ebenfalls zu einem Fortschreiten (Progression) einer chronischen Nierenerkrankung führt.

Hohe Harnsäurewerte sind schlecht für die Nieren
Wer sich säurebildend ernährt, nimmt allgemein auch mehr Purine (siehe Kasten) zu sich als Menschen, die basische Lebensmittel bevorzugen. Entsprechend ist die Harnsäurekonzentration im Blut unter einer säurelastigen Ernährung höher (Hyperurikämie) als unter einer basischen Diät.
Allerdings fördert ein basischer Urin die Harnsäureausscheidung und damit die sogenannte Harnsäure-Clearance. Wie eine Studie gezeigt hat, war in der Gruppe mit säurebildender Nahrung (proteinreich und gemüsearm)
- die Harnsäurekonzentration im Blut höher,
- die Harnsäurekonzentration im Urin allerdings niedriger
als in der Gruppe, die eine basische Diät (proteinärmer und gemüsereich) verzehrt hatte.
Die Forschenden schlossen daraus, dass der Körper Harnsäure aus saurem Urin aktiver rückresorbiert als bei alkalischem Urin.
Das bedeutet, eine säurebildende Ernährung erhöht das Risiko
- für Gicht doppelt:
- durch erhöhte Harnsäurewerte im Blut: bei einer Übersättigung kristallisiert die Harnsäure
- durch Ansäuerung des Körpers, wodurch Harnsäurekristalle noch leichter ausfallen
- für Nierensteine in Form von Harnsäuresteinen, die sich im sauren Urin ebenfalls verstärkt bilden (siehe unten).
Purinreiche Ernährung fördert die Harnsäurebildung
Wenn der Körper Purine abbaut, entsteht Harnsäure, die er in der Regel mit dem Urin ausscheidet. Purine sind Bestandteile der Nukleinsäuren, die DNA und RNA aufbauen. Sie stammen zum einen aus dem eigenen Körper, zum anderen aus der Ernährung. Insbesondere Fleisch, aber auch Hülsenfrüchte und Bier sind purinreich. Auch Kohl, Spargel und Schokolade enthalten viele Purine.
Allerdings tragen manche Medikamente ebenfalls zu einem erhöhten Harnsäurespiegel bei, wie beispielsweise Entwässerungsmittel (Diuretika).
Indessen scheint die Harnsäure die Nieren auch direkt zu schädigen, nicht allein durch die Bildung von Harnsäuresteinen. So fand eine Übersichtsarbeit (Metaanalyse), die 15 Studien umfasst, einen positiven Zusammenhang zwischen dem Harnsäurespiegel im Blut und dem Risiko für das Auftreten einer chronischen Nierenerkrankung bei Menschen mittleren Alters. Dieser Zusammenhang war unabhängig von bekannten stoffwechselbedingten Risikofaktoren.
Eine aktuellere chinesische Metaanalyse zeigte, dass jeder Anstieg der Harnsäurekonzentration um 1 mg/dl mit einem um 49 Prozent erhöhten Risiko für eine CKD verbunden war. Zudem bestätigte die Übersichtsarbeit dies auch für ältere Erwachsene. Insbesondere bei Männern ist das Risiko erhöht, wie eine japanische Studie ergab.
Nierenschwäche verursacht Azidose und erhöht das Sterberisiko
Wenn die Nierenfunktion nachlässt, kann weniger Säure aus dem Körper ausgeschieden werden. Damit gerät der Säure-Basen-Haushalt aus dem Gleichgewicht: Er wird ins Saure verschoben. Das verstärkt eine chronisch latente Übersäuerung und kann – bei ausgeprägter Nierenschwäche (oder einer diabetischen Ketoazidose) – eine manifeste metabolische Azidose auslösen, bei der auch der pH-Wert des Blutes unter 7,35 sinkt. Damit entsteht ein Teufelskreis: Die eingeschränkte Nierenfunktion führt zu einer Übersäuerung und diese beeinträchtigt die Nieren weiter.
Die Gesundheit von Menschen mit einer chronischen Nierenerkrankung (CKD), die an einer damit einhergehenden metabolischen Azidose leiden, ist doppelt gefährdet:
- Bei bestehender Nierenschädigung beschleunigt eine säurebildende Ernährung das Fortschreiten der Erkrankung und erhöht das Risiko eines terminalen Nierenversagens. Hierbei kann der Bicarbonatspiegel im Blut als Marker dienen, denn eine Studie ergab, dass niedrige Serum-Bicarbonatwerte – unabhängig von der Ausgangs-eGFR – mit dem Fortschreiten einer Nierenerkrankung verbunden sind.
- Zudem haben die Betroffenen ein erhöhtes Risiko für schwerwiegende kardiovaskuläre Ereignisse: Herzinsuffizienz, Schlaganfall, Myokardinfarkt und Tod durch Herz-Kreislauf-Erkrankungen.
Jeder Anstieg des Serum-Bicarbonats um 1 Milliäquivalent (mEq/l) führte in einer Studie dagegen zu einer Risikoreduktion von 4 Prozent.
Geschädigte Nieren haben Konsequenzen für den ganzen Körper
Funktionieren unsere Nieren nur eingeschränkt, wirkt sich dies auf den gesamten Organismus aus:
- Bluthochdruck und ein Ungleichgewicht des Elektrolythaushalts können auftreten und in der Folge akute Herz-Kreislauf-Erkrankungen wie Herzinfarkt und Schlaganfall auslösen. Dabei ist das Risiko für Herz-Kreislauf-Komplikationen bereits in frühen Stadien der chronischen Nierenerkrankung erhöht.
- Manifeste Übersäuerung (metabolische Azidose): Symptome sind Übelkeit und Erbrechen, aber auch Müdigkeit und Schwäche sowie Kopfschmerzen. Durch eine tiefe, schnelle Atmung (Kussmaul-Atmung) versucht der Körper, Säure – in Form von CO2 – loszuwerden.
Langfristig leiden besonders die Knochen unter der Übersäuerung, da der Körper Puffersubstanzen gewinnt, indem er Mineralstoffe aus ihnen löst. - Knochenschäden: Gesunde Nieren können Vitamin D in seine aktive Form (Calcitriol) umwandeln. Dieses fördert starke Knochen, da es für den Einbau von Calcium in die Knochen sorgt. Bei Nierenschwäche ist weniger Calcitriol vorhanden. In der Folge lagern die Knochen weniger Calcium ein und werden brüchig.
- Nervenschäden: Bei einer chronischen Nierenerkrankung können die Nieren weniger Abfall- und Giftstoffe ausscheiden. Diese sammeln sich im Blut an und können auch die Nerven und das Gehirn schädigen.
Übersäuerung begünstigt Nierensteine
Viele Menschen haben Nierensteine, die – abhängig von ihrer Größe – mal mehr, mal weniger Probleme bereiten.
Was sind Nierensteine?
Bei Nierensteinen handelt es sich um auskristallisierte Mineralstoffe, die sich als kleinere oder größere „Steine“ in der Niere oder den ableitenden Harnwegen („Harnleitersteine“) ablagern. Oft bleiben sie unbemerkt und werden in der Regel mit dem Urin ausgeschieden. Wenn sie zu groß werden, können sie allerdings Probleme bereiten: Sie können mechanische Verletzungen auslösen oder sogar den Abfluss des Harns blockieren und Entzündungen verursachen. Das führt zu Blut im Urin und Schmerzen, die auch heftig ausfallen können (Nierenkolik).
Mindestens 10 Prozent aller Menschen haben einmal im Leben Nieren- oder Harnleitersteine. Dabei sind mehr Männer als Frauen betroffen.
Nierensteine können aus verschiedenen Mineralien bestehen:
- 80 Prozent sind Calciumsteine, meist als Calciumoxalat, aber auch Calciumphosphat.
- 5 bis 10 Prozent sind Harnsäuresteine, die mit Gicht zusammenhängen.
Lebensmittel, die viel Oxalat enthalten – wie zum Beispiel Rhabarber, Algen, Baumnüsse und Spinat, aber auch Schokolade – begünstigen die Bildung von Steinen aus Calciumoxalat.
Vorbeugen kann man Nierensteinen, indem man viel trinkt und seine Ernährung umstellt.
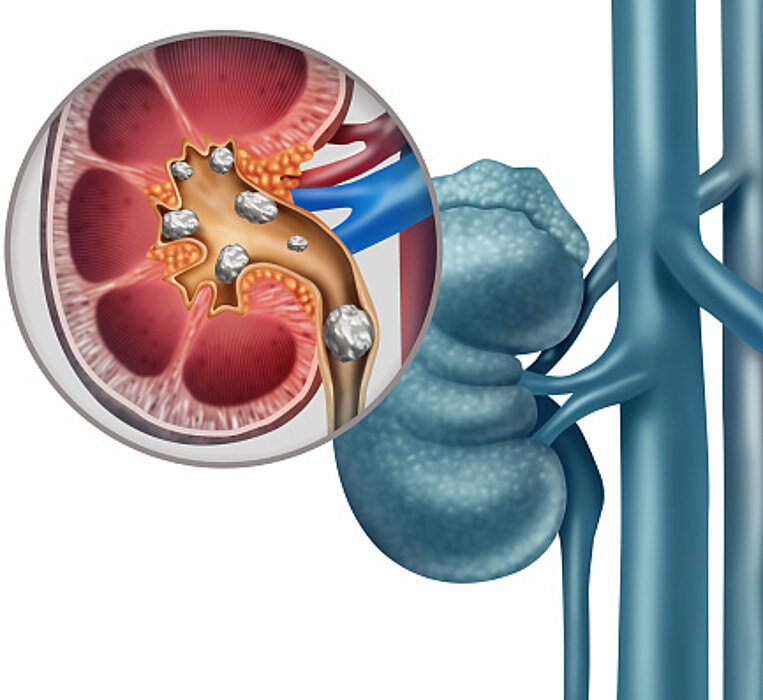
Ist der Körper chronisch übersäuert, kommt es zu einer verminderten Citrat-Ausscheidung. Dadurch wird der Urin sauer – und das Risiko für Nierensteine steigt, da Calciumphosphat und Harnsäure im sauren Milieu verstärkt auskristallisieren.
Die verringerte Citrat-Ausscheidung mit dem Urin ist daher ein sensitiver, nicht invasiver Marker für Veränderungen des systemischen (den ganzen Körper betreffenden) Säurehaushalts und gleichzeitig ein Risikofaktor für die Bildung von Nierensteinen.
Wie Studien gezeigt haben, weisen Menschen mit Nierensteinen oft eine erhöhte Säurebelastung aufgrund ihrer Ernährung auf: Sie verzehren zu wenig Gemüse und sind dadurch nur mangelhaft mit Basen versorgt. Dagegen kann eine basenreiche Ernährung beziehungsweise eine Therapie mit Basen das Risiko für eine erneute Steinbildung bei Patientinnen und Patienten deutlich – um mehr als das Fünffache – verringern.
In diesem Zusammenhang ist von Bedeutung, dass ein erhöhter Body-Mass-Index (BMI) und das Risiko für Nierensteine – zumindest bei Erwachsenen – anscheinend zusammenhängen. Denn Übergewicht und BMI werden ebenfalls durch die Ernährung und eine erhöhte Säurebelastung beeinflusst.
Säurebelastung verringert nierenschützendes Uromodulin
Das häufigste Eiweiß im Urin ist bei gesunden Menschen – mit etwa 40–50 Prozent –Uromodulin, das ausschließlich in den Nieren produziert wird. Es schützt vor
- der Bildung von Nierensteinen, indem es die Zusammenlagerung (Aggregation) von Calciumoxalat und Calciumphosphat unterbindet.
- Harnwegsinfekten, indem es Bakterien bindet und so deren Anhaften an die Harnwege verhindert.
Uromodulin dient auch als Marker für die Nierenfunktion.
Wie eine Studie gezeigt hat, hängt die Menge an Uromodulin bei gesunden 3- bis 17-Jährigen umgekehrt mit der Netto-Säureausscheidung (NAE) und positiv mit dem pH-Wert des Urins zusammen. Das bedeutet, es ist mehr Uromodulin vorhanden
- wenn die NAE niedrig ist,
- der pH-Wert des Urins hoch ist.
Daraus schlossen die Forschenden, dass das durch eine hohe endogene Säureproduktion erhöhte Risiko für Harnsteine durch die Abnahme von Uromodulin weiter verstärkt werden könnte.
Nierensteine schon bei Kindern
In den letzten Jahren sehen ärztliche Fachleute eine Zunahme an Steinen – besonders aus Calciumoxalat und Calciumphosphat – und das auch bei Kindern. Die Gründe:
- Eine verminderte Citrat-Ausscheidung (Hypocitraturie) – aufgrund höherer Mengen an Cortisol – säuert den Urin an und lässt die Mineralien schneller auskristallisieren.
Bei gesunden Kindern beeinflussen selbst mäßig erhöhte Cortisolwerte, die noch im physiologischen Bereich liegen, die Citrat-Ausscheidung über die Nieren negativ: Je höher die Cortisolwerte sind, desto geringer die Citrat-Konzentration im Urin. Erhöhte Cortisolwerte können sowohl durch anhaltenden Stress als auch durch eine dauerhafte Säurebelastung des Körpers verursacht werden.
- Eine verstärkte Ausscheidung von Calcium mit dem Urin (Hypercalciurie): Diese kann durch eine hohe Natrium- oder Proteinzufuhr verschlimmert werden. Denn Calcium wird gerade bei einer Übersäuerung des Körpers verstärkt aus den Knochen freigesetzt und mit dem Urin ausgeschieden.
- Ein Fünftel der Kinder weist auch eine übermäßige Ausscheidung von Oxalat (Hyperoxalurie) auf. Ursache kann ein erhöhter Verzehr oxalatreicher Lebensmittel bei gleichzeitiger geringer Calciumzufuhr sein, da so die Oxalataufnahme aus dem Darm gefördert wird.
Ernährungsumstellung, Mikronährstoffe und Basenpräparate
Eine Ernährungsumstellung von überwiegend säurebildenden auf reichlich basische Lebensmittel und auch die Einnahme von Basenpräparaten mindert die Säurebelastung für den Körper und führt zu einer Verbesserung der Säureausscheidung. Das kann dazu beitragen, die Entwicklung einer chronischen Nierenerkrankung zu verhindern beziehungsweise ihr Fortschreiten zu bremsen. Laut einer Studie ließen sowohl viel Obst und Gemüse als auch der Verzehr von Bicarbonat die Urin-Marker für Nierenschäden – wie beispielsweise Eiweiß im Urin – bei Menschen mit Nierenerkrankung sinken. Damit verlangsamte sich auch der Rückgang der geschätzten glomerulären Filtrationsrate (eGFR).
In pflanzlichen Lebensmitteln kommen organische Säuren beziehungsweise ihre Anionensalze wie Citronensäure und Citrat oder auch Äpfelsäure und Malat vor. Sie führen zur Bildung von Bicarbonat, die als wichtigste Puffersubstanz im Blut fungiert.

Basenpräparate auf Citrat-Basis vorteilhaft
Eine Unterstützung durch hochwertige Basenpräparate ist ebenfalls sinnvoll, da sie basische Mineralstoffe und Anionen – Bicarbonat oder Citrat – liefern. (Natrium-)Bicarbonat (Natriumhydrogencarbonat = NaHCO₃) – auch als Natron bezeichnet – konnte in verschiedenen Studien das Fortschreiten einer Nierenerkrankung verhindern. Da eine Steigerung der Natriumzufuhr den Blutdruck erhöhen kann, sollte besser zu Mikronährstoffpräparaten mit Magnesium, Kalium und Calcium gegriffen werden, die idealerweise mit Citrat kombiniert sind. Während Bicarbonat schon im Magen die Säure neutralisieren kann und deshalb gerne bei Sodbrennen eingesetzt wird, ist Citrat erst nach Aufnahme aus dem Darm ins Blut wirksam und hilft dort, Bicarbonat zu bilden.
Die Einnahme von Citrat-Präparaten kann den Urin basischer machen und die renale Ausscheidung von Harnsäure fördern, wie eine Studie belegt hat: Menschen mit erhöhten Harnsäurewerten, die zusätzlich zu einem Harnsäuresenker (Allopurinol) ein Citrat-Präparat einnahmen, erfuhren eine stärkere Senkung ihrer Harnsäurewerte als die Personen, die nur Allopurinol bekamen. Ihr Urin war deutlich basischer. Zudem zeigte eine Untergruppe, die eine eingeschränkte Nierenfunktion besaß, bei Citrat-Einnahme eine signifikant erhöhte Kreatinin-Clearance. Dies steht für eine verbesserte glomeruläre Filtrationsrate, also eine bessere Nierenfunktion.
Nierenschutz bei Nierenschwäche
Zum Fortschreiten einer chronischen Nierenerkrankung tragen mehrere Faktoren bei, unter anderem:
- Säurestress
- ein gestörtes Darmmikrobiom: Eine hohe Zufuhr tierischer Proteine verändert das Darmmikrobiom negativ und sorgt unter anderem für eine hohe Ammoniak-Belastung der Leber. Diese wird durch die verstärkte Ammoniak-Entgiftung überfordert und Ammoniak reichert sich im Blut an. Dadurch muss es über die Nieren entgiftet werden, was diese schädigen kann.
- oxidativer Stress – zum Beispiel durch Rauchen

Im Umkehrschluss bedeutet dies, dass wir mit einem gesunden Lebensstil – insbesondere einer pflanzenbasierten, basischen Ernährung – unsere Nieren schützen und das Fortschreiten einer Nierenschwäche aufhalten oder zumindest verlangsamen können. Insbesondere die Minderung von Säurestress wirkt nierenschützend – auch dann, wenn noch keine manifeste metabolische Azidose vorliegt.
Vor allem Menschen, die bereits an einer Nierenschwäche leiden, profitieren von einer basischen Ernährung: Ein reduzierter Eiweißgehalt der Nahrung und ein erhöhter Verzehr pflanzlicher Kost kann die Säurebelastung des Körpers verringern und den Rückgang der glomerulären Filtrationsrate verlangsamen, wie Studien gezeigt haben.
Nierensteine durch gezielte Ernährungsstrategien verhindern
Gezielte Ernährungsumstellungen können das Risiko der Harnsteinbildung und ihres Wiederauftretens verringern:
- Wichtig ist es, insbesondere die Flüssigkeitszufuhr zu steigern, um eine tägliche Urinausscheidung von etwa 2 Litern zu erzielen. Ist der Körper dehydriert, fördert dies die Bildung von Steinen.
(Hinweis: Liegt bereits eine deutliche Nierenschädigung vor, die Trinkmenge ärztlich abklären.) - Eine basische Ernährung kann den Harnsäurespiegel und damit das Risiko für Harnsäuresteine sowie für Gicht senken.
- Menschen mit Nierensteinen, die eine Hypocitraturie (also zu wenig Citrat im Urin) aufweisen, können basische (alkalische) Citrat-Lösungen verzehren, um die Citrat-Menge im Körper zu steigern.
- Eine basische Ernährung, also der erhöhte Verzehr von Obst und Gemüse (keine oxalatreichen Sorten), steigert ebenfalls die Citrat-Ausscheidung und kann signifikant vor Nierensteinbildung schützen. Besonders Zitrusfrüchte (Zitronen, Orangen, Grapefruits und Limetten), aber auch andere Früchte (Melonen, Äpfel, Beeren sowie Tomaten, Paprika) sind natürliche Quellen für Citrat. Studien belegen das Potenzial dieser Früchte beziehungsweise ihrer Säfte, den Citrat-Spiegel im Urin zu erhöhen. Citrat bindet gelöstes Calcium im Urin und verhindert, dass sich Calciumkristalle bilden.
In einer Studie zeigte sich ein signifikant schützender Effekt vor Nierensteinen durch mindestens zwei Gemüseportionen pro Tag.
- Wenn viele Steine aus Calciumoxalat vorliegen, ist eine oxalatarme Ernährung und/oder eine normale bis hohe Calciumzufuhr (800–1200 mg/Tag für Erwachsene) sinnvoll. Oxalat (Rhabarber etc.) sollte am besten immer zusammen mit calciumreichen Milchprodukten (Sahne, Pudding, Milcheis) verzehrt werden. Dann bildet sich Calciumoxalat schon im Darm und das Oxalat wird nicht resorbiert, sondern über den Stuhl ausgeschieden.
- Eine diätetische Calciumrestriktion wird nicht empfohlen, im Gegenteil: Eine calciumreiche Ernährung (≥ 1 g/Tag) mit niedrigem Protein- und Natriumgehalt kann das Risiko der Steinbildung verringern. Eine niedrige, aber normale Proteinzufuhr senkt die Calciumausscheidung. Ein moderater Salzverzicht (Natriumrestriktion) kann die Calcium-Ausscheidung im Urin ebenfalls begrenzen.
- Dagegen steigert eine proteinreiche Ernährung das Risiko für Steine aus Calciumoxalat, da die Calciumausscheidung zunimmt, gleichzeitig aber weniger Citrat ausgeschieden wird. Ein hoher Proteinverzehr steigert die Säurebelastung des Körpers und führt zu einer verstärkten Ausscheidung von Calcium, das zuvor aus den Knochen gelöst wurde.
Zum Abnehmen wird oft eine kohlenhydratarme, aber proteinreiche Diät empfohlen. Diese führt allerdings zu einer deutlichen Säurebelastung des Körpers und der Nieren, verschlechtert die Calciumbilanz und erhöht das Risiko der Nierensteinbildung sowie für Knochenschwund. - Auch ein hohes Verhältnis von tierischem Protein zu Kalium ist mit einem erhöhten Risiko der Nierensteinbildung verbunden. Ein relativ hoher Kaliumanteil im Vergleich zu tierischem Eiweiß könnte eine Möglichkeit zur Vorbeugung darstellen.
Zusammenfassung
Die beiden Nieren spielen eine wichtige Rolle im Säure-Basen-Haushalt, da sie als einziges Organ Säuren in relevanter Menge direkt ausscheiden können. Das ist insbesondere für nicht flüchtige Säuren und bei einer übermäßigen Säurebelastung von Bedeutung. Zudem gewinnen die Nieren das wichtige Bicarbonat aus dem Primärharn zurück und können auch neues Bicarbonat bilden.
Mit dem Alter lässt die Nierenfunktion allerdings nach. Dann kann auch weniger Säure aus dem Körper entfernt werden – und das Risiko für eine manifeste Azidose steigt.
Eine chronische Nierenerkrankung (CKD) wird durch Bluthochdruck und hohe Blutzuckerwerte befeuert. Aber auch eine chronische latente Übersäuerung des Körpers beeinträchtigt die Nierenfunktion. Hieran ist vor allem das giftige Ammoniak schuld, das bei einer hohen Säurelast verstärkt in den Nieren gebildet wird. Durch die Übersäuerung erhöhte Aldosteronwerte sorgen zudem für eine verstärkte Fibrose, also einen Umbau des Nierengewebes zu funktionslosem Bindegewebe. Daneben führt eine übermäßige Belastung mit Harnsäure – die vielfach aufgrund einer verbreiteten purinreichen Ernährung besteht – ebenfalls zu einem Rückgang der glomerulären Filtrationsrate (GFR) und zum Fortschreiten einer chronischen Nierenerkrankung.
Ist der Körper latent übersäuert, sinkt die Citrat-Ausscheidung und der Urin wird sauer. Dann kann weniger Harnsäure ausgeschieden werden, aber im Gegenzug können vermehrt Kristalle ausfallen, vor allem aus Calciumoxalat und Harnsäure. Große Nierensteine können den Urinabfluss behindern und Schmerzen verursachen.
Um sich vor Nierensteinen zu schützen, ist eine Ernährungsumstellung sinnvoll. Dazu zählt insbesondere ein vermehrter Verzehr von Basen und auch Calcium, aber eine geringere Zufuhr säurebildender und oxalatreicher Lebensmittel.
Eine basenreiche Ernährung und Basenpräparate können die Nierengesundheit in mehrfacher Hinsicht fördern: Sie machen den Urin basischer und können die Säure- und Harnsäureausscheidung verbessern, den Rückgang der Nierenfunktion bremsen und das Risiko für Nierensteine senken. Hochwertige Basenpräparate versorgen den Körper mit basischen Komponenten: Magnesium, Kalium und Calcium sowie Citrat.
Verzeichnis der Studien und Quellen
Adeva MM et al. (2012): Ammonium metabolism in humans. Metabolism. https://www.sciencedirect.com/science/article/abs/pii/S0026049512002703
Alfandary et al. (2018): Increasing Prevalence of Nephrolithiasis in Association with Increased Body Mass Index in Children: A Population Based Study. J Urol. https://www.auajournals.org/doi/10.1016/j.juro.2017.10.023
Banerjee T et al. (2014): Dietary acid load and chronic kidney disease among adults in the United States. BMC Nephrol. https://bmcnephrol.biomedcentral.com/articles/10.1186/1471-2369-15-137
Berkemeyer S et al. (2008): Renal Net Acid Excretion Capacity Is Comparable in Prepubescence, Adolescence, and Young Adulthood but Falls with Aging. J Am Geriatr Soc. https://agsjournals.onlinelibrary.wiley.com/doi/10.1111/j.1532-5415.2008.01799.x
Collister D et al. (2021): Metabolic Acidosis and Cardiovascular Disease in CKD. Kidney Med. https://pmc.ncbi.nlm.nih.gov/articles/PMC8551483/
Copelovitch L (2012): Urolithiasis in Children: Medical Approach. Pediatr Clin North Am. https://www.sciencedirect.com/science/article/pii/S003139551200082X
de Brito-Ashurst I et al. (2009): Bicarbonate Supplementation Slows Progression of CKD and Improves Nutritional Status. J Am Soc Nephrol. https://pmc.ncbi.nlm.nih.gov/articles/PMC2736774/
Derakhshandeh-Rishehri SM et al. (2024): Higher Renal Net Acid, but Not Higher Phosphate Excretion During Growth Associates With Lower Adult Circulating Uromodulin. J Ren Nutr. https://www.jrnjournal.org/article/S1051-2276(24)00285-1/fulltext
Deutsche Gesellschaft für Nephrologie (16.09.2025): Warum Blutdruck und Blutzucker entscheidend für die Nierengesundheit sind. https://www.dgfn.eu/pressemeldung/warum-blutdruck-und-blutzucker-entscheidend-fuer-die-nierengesundheit-sind.html, zuletzt abgerufen am 14.04.2026.
Deutsches Ärzteblatt (10.11.2025): Fast 800 Millionen Menschen von chronischer Nierenkrankheit betroffen. https://www.aerzteblatt.de/news/fast-800-millionen-menschen-von-chronischer-nierenkrankheit-betroffen-c0fb5a9a-99ae-49b4-b1c2-71c68ccb211d, zuletzt abgerufen am 14.04.2026.
Deutsches Ärzteblatt (17.07.2020): Uromodulin – wie ein Protein aus den Nieren Harnwegsinfektionen verhindert. https://www.aerzteblatt.de/news/uromodulin-wie-ein-protein-aus-den-nieren-harnwegsinfektionen-verhindert-3f1a1f7d-e930-4271-bc0c-4db878e17d5c, zuletzt abgerufen am 14.04.2026.
DKV (o. D.): Niereninsuffizienz – wenn die Nieren noch eingeschränkt funktionieren. https://www.dkv.com/gesundheit-themenwelt-innere-organe-niereninsuffizienz-wenn-die-nieren-noch-eingeschraenkt-funktionieren.html, zuletzt abgerufen am 14.04.2026.
DocCheck Flexikon (06.08.2025): Ammoniummechanismus. https://flexikon.doccheck.com/de/Ammoniummechanismus, zuletzt abgerufen am 14.04.2026.
DocCheck Flexikon (03.02.2024): Aufgabe der Niere im Säure-Basenhaushalt. https://flexikon.doccheck.com/de/Aufgabe_der_Niere_im_S%C3%A4ure-Basenhaushalt, zuletzt abgerufen am 14.04.2026.
DocCheck Flexikon (23.11.2025): Glomeruläre Filtrationsrate. https://flexikon.doccheck.com/de/Glomerul%C3%A4re_Filtrationsrate, zuletzt abgerufen am 14.04.2026.
DocCheck Flexikon (21.03.2024): Harnstoffzyklus. https://flexikon.doccheck.com/de/Harnstoffzyklus, zuletzt abgerufen am 14.04.2026.
DocCheck Flexikon (19.11.2017): Natriumhydrogencarbonat. https://flexikon.doccheck.com/de/Natriumhydrogencarbonat, zuletzt abgerufen am 14.04.2026.
DocCheck Flexikon (21.03.2024): Nephron. https://flexikon.doccheck.com/de/Nephron, zuletzt abgerufen am 14.04.2026.
DocCheck Flexikon (05.02.2025): Säure-Basen-Haushalt. https://flexikon.doccheck.com/de/S%C3%A4ure-Basen-Haushalt, zuletzt abgerufen am 14.04.2026.
DocCheck Flexikon (24.06.2025): Tamm-Horsfall-Protein. https://flexikon.doccheck.com/de/Tamm-Horsfall-Protein, zuletzt abgerufen am 14.04.2026.
Esche J et al. (2018): Dietary Potential Renal Acid Load Is Positively Associated with Serum Uric Acid and Odds of Hyperuricemia in the German Adult Population. J Nutr. https://www.sciencedirect.com/science/article/pii/S0022316622108679
Esche J et al. (2020): Estimates of renal net acid excretion and their relationships with serum uric acid and hyperuricemia in a representative German population sample. Eur J Clin Nutr. https://www.nature.com/articles/s41430-020-0688-2
Fellström B et al. (1984): Effects of high intake of dietary animal protein on mineral metabolism and urinary supersaturation of calcium oxalate in renal stone formers. Br J Urol. https://pubmed.ncbi.nlm.nih.gov/6544608/
Ferraro et al. (2016): Dietary Protein and Potassium, Diet–Dependent Net Acid Load, and Risk of Incident Kidney Stones. Clin J Am Soc Nephrol. https://journals.lww.com/cjasn/abstract/2016/10000/dietary_protein_and_potassium,_diet_dependent_net.17.aspx
Garza FA & Leslie (2025): Anatomy, Abdomen and Pelvis: Kidneys. StatPearls. https://pubmed.ncbi.nlm.nih.gov/29494007/
gesund.bund.de (22.09.2025): Chronische Nierenerkrankung. https://gesund.bund.de/chronische-nierenerkrankung#haeufigkeit, zuletzt abgerufen am 14.04.2026.
gesundheit.gv.at (25.11.2024): Bikarbonat. https://www.gesundheit.gv.at/labor/laborwerte/blutgase-saeure-basen-haushalt/labor-bikarbonat-bik1.html, zuletzt abgerufen am 14.04.2026.
gesundheitsinformation.de (20.03.2025): Harnsäure. https://www.gesundheitsinformation.de/harnsaeure.html, zuletzt abgerufen am 14.04.2026.
gesundheitsinformation.de (22.02.2023): Nierensteine und Harnleitersteine. https://www.gesundheitsinformation.de/nierensteine-und-harnleitersteine.html, zuletzt abgerufen am 14.04.2026.
gesundheitsinformation.de (22.02.2023): Vorbeugung von Nierensteinen. https://www.gesundheitsinformation.de/vorbeugung-von-nierensteinen.html, zuletzt abgerufen am 14.04.2026.
Goraya N & Wesson (2020): Novel dietary and pharmacologic approaches for acid-base modulation to preserve kidney function and manage uremia. Curr Opin Nephrol Hypertens. https://europepmc.org/article/med/31725012
Goraya N et al. (2012): Dietary acid reduction with fruits and vegetables or bicarbonate attenuates kidney injury. Kidney Int. https://www.kidney-international.org/article/S0085-2538(15)55178-8/fulltext
Goraya N et al. (2018): Acid retention in chronic kidney disease is inversely related to GFR. Am J Physiol. https://journals.physiology.org/doi/full/10.1152/ajprenal.00463.2017
Hamm LL et al. (2015): Acid-Base Homeostasis. Clin J Am Soc Nephrol. https://pmc.ncbi.nlm.nih.gov/articles/PMC4670772/
Hua et al. (2020): Cortisol and determinants of renal citrate excretion. Endocrine. https://link.springer.com/article/10.1007/s12020-019-02151-0
Huang Y et al. (2025): Metabolic syndrome and CKD risk. BMC Endocr Disord. https://pmc.ncbi.nlm.nih.gov/articles/PMC12121056/
Kanbara A et al. (2012): Urine pH and uric acid clearance. Nutr J. https://link.springer.com/article/10.1186/1475-2891-11-39
Krupp D et al. (2018): Citrate excretion and blood pressure. Am J Physiol. https://journals.physiology.org/doi/full/10.1152/ajprenal.00144.2018
Lin S et al. (2025): Gut microbial ammonia metabolism and CKD. Nat Microbiol. https://www.nature.com/articles/s41564-025-02039-y
München Klinik (14.03.2019): Unsere Nieren – Kläranlage und Kraftpaket. https://www.muenchen-klinik.de/meldungen-nachrichten/meldungen-nachrichten/artikel/unsere-nieren-klaeranlage-und-kraftpaket/, zuletzt abgerufen am 14.04.2026.
Osuna-Padilla IA et al. (2019): Dietary acid load. Nefrologia. https://www.revistanefrologia.com/es-dietary-acid-load-mechanisms-evidence-articulo-S2013251419301129
Pecoraro et al. (2024): Pediatric Nephrolithiasis. Medicina. https://pmc.ncbi.nlm.nih.gov/articles/PMC11728360/
Prezioso D et al. (2015): Dietary treatment of urinary risk factors. Arch Ital Urol Androl. https://www.pagepressjournals.org/index.php/aiua/article/view/aiua.2015.2.105
Reddy ST et al. (2002): High-protein diets and acid-base balance. Am J Kidney Dis. https://www.ajkd.org/article/S0272-6386(02)00039-2/abstract
Rodriguez Neto Angeloco L et al. (2018): Alkaline diet and CKD. J Ren Nutr. https://www.jrnjournal.org/article/S1051-2276(17)30257-1/abstract
Saito J et al. (2010): Citrate reduces uric acid levels. Endocr Res. https://pmc.ncbi.nlm.nih.gov/articles/PMC3413920/
Schmitt R (2022): Blockierung des Renin-Angiotensin-Aldosteron-Systems. Die Nephrologie. https://link.springer.com/article/10.1007/s11560-021-00525-y
Scialla JJ & Anderson (2013): Dietary acid load in CKD. Adv Chronic Kidney Dis. https://pmc.ncbi.nlm.nih.gov/articles/PMC3604792/
Seifi N et al. (2024): Acid load and hyperuricemia. Int Urol Nephrol. https://link.springer.com/article/10.1007/s11255-023-03876-8
Shah SN et al. (2009): Serum bicarbonate and CKD progression. Am J Kidney Dis. https://pmc.ncbi.nlm.nih.gov/articles/PMC4354889/
Smeijer et al. (2025): Endothelin receptor antagonists in CKD. Nat Rev Nephrol. https://www.nature.com/articles/s41581-024-00908-z
Sromicki J et al. (2022): Renal tubular acidosis and nephrolithiasis. J Nephrol. https://link.springer.com/article/10.1007/s40620-021-01207-7
Stradtmann H (2017): Metabolische Azidose. Dialyse aktuell. https://www.thieme-connect.com/products/ejournals/pdf/10.1055/s-0043-116642.pdf
Trinchieri A et al. (2013): Acid load and kidney stones. Eur J Clin Nutr. https://www.nature.com/articles/ejcn2013155
Universitätsklinikum Leipzig (o. D.): Chronische Niereninsuffizienz. https://www.uniklinikum-leipzig.de/einrichtungen/medizinische-klinik-3/Seiten/einteilung.aspx, zuletzt abgerufen am 14.04.2026.
Universitätsspital Zürich (22.10.2025): Chronische Nierenerkrankung. https://www.usz.ch/krankheit/chronische-nierenerkrankung/, zuletzt abgerufen am 14.04.2026.
Urologische Stiftung Gesundheit (o. D.): Was bedeutet hohe Harnsäure? https://urologische-stiftung-gesundheit.de/haeufige-fragen/was-bedeutet-hohe-harnsaeure/, zuletzt abgerufen am 14.04.2026.
Vallet M et al. (2015): Urinary ammonia and CKD outcomes. Kidney Int. https://www.sciencedirect.com/science/article/pii/S2157171615321432
Vetter C (2014): Hyperurikämie und Niere. Dialyse aktuell. https://www.thieme-connect.com/products/ejournals/html/10.1055/s-0034-1366967
Vezzoli et al. (2015): Dietary style and acid load. Nutr Metab Cardiovasc Dis. https://www.nmcd-journal.com/article/S0939-4753(15)00061-7/abstract
vorsorge-online.de (23.01.2024): Nierenversagen – jeder fünfte Fall wegen Bluthochdruck. https://www.vorsorge-online.de/magazin/vorsorge-in-zahlen/details/nierenversagen-jeder-fuenfte-fall-wegen-bluthochdruck/, zuletzt abgerufen am 14.04.2026.
Wesson DE et al. (2011): Acid retention and GFR. Am J Physiol. https://journals.physiology.org/doi/full/10.1152/ajprenal.00587.2010
Wu N et al. (2021): Uric acid and CKD risk. Nutr Metab. https://link.springer.com/article/10.1186/s12986-021-00618-4
Yamada T et al. (2011): Uric acid predicts CKD. Am J Med Sci. https://www.amjmedsci.org/article/S0002-9629(15)31101-0/abstract
Zhu P et al. (2014): Uric acid and CKD meta-analysis. PLoS One. https://pmc.ncbi.nlm.nih.gov/articles/PMC4069173/