Bei Stress sowie seelischer und körperlicher Belastung produziert die Nebenniere Stresshormone wie Cortisol. In der akuten Situation ist diese Reaktion hilfreich, doch wenn der Stress chronisch wird, können die Nebennieren erschöpfen. Der Körper stellt sich dann auf Belastungen nicht mehr ein und reagiert mit Müdigkeit. Zu der Stressreduktion im Alltag sind Mikronährstoffe wichtig. Sie können vor Stress schützen und die Regeneration der natürlichen Stressantwort verbessern. Lesen Sie hier, welche Vitamine, Mineralstoffe und Aminosäuren die Nebenniere unterstützen können.
Ursachen und Symptome
Was ist eine Nebennierenschwäche?
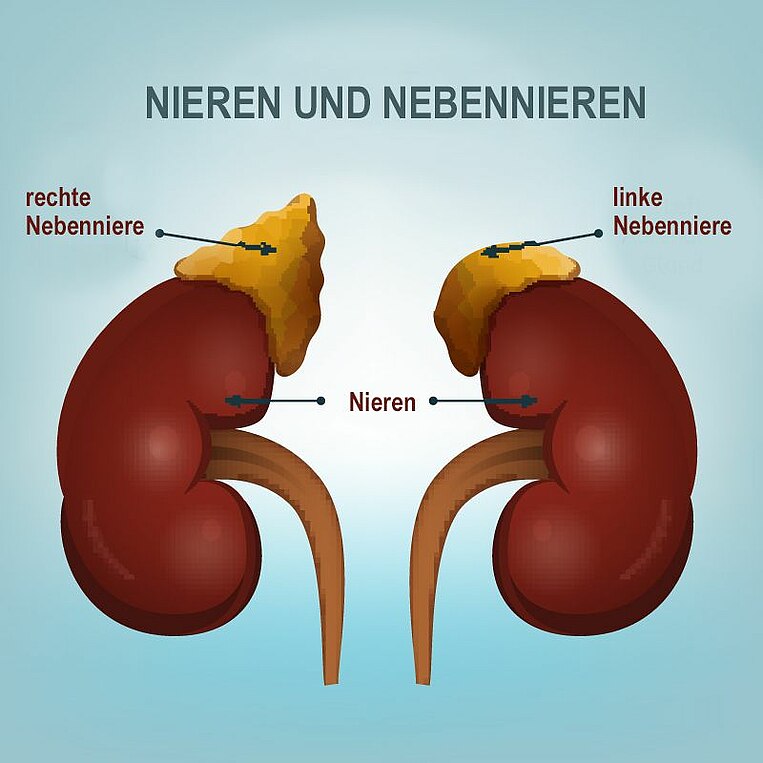
Die Nebennieren produzieren verschiedene aktivierende Hormone und Botenstoffe für das Nervensystem (Neurotransmitter) und den Stoffwechsel. Diese haben zahlreiche Wirkungen und bereiten den Körper unter anderem auf Anstrengung und Stress vor. Man bezeichnet die Unterfunktion der Nebennieren als Nebennierenschwäche (englisch: adenal fatigue).
Bei Nebennierenschwäche werden folgende Hormonsysteme behindert:
- Stresshormone wie Cortisol oder Adrenalin. Das beeinträchtigt die Energiebereitstellung und die Blutzuckerregulation, was wiederrum zu Müdigkeit und Hunger führt.
- Hormone für den Wasser- und Salzhaushalt wie Aldosteron und Cortisol. Dadurch fällt der Blutdruck. Betroffenen wird beim Aufstehen schwarz vor Augen. Sie haben oft ein starkes Verlangen nach Salz.
- Vorläufer der Geschlechtshormone Testosteron und Östrogen (Dehydroepiandrosteron (DHEA)). Dadurch werden die Sexualfunktion und der Stoffwechsel beeinträchtigt.
- Der Hormonvorläufer Pregnenolon. Aus ihm werden viele andere Hormone hergestellt wie Stress-, Mineralstoff- und Blutdruckhormone. Pregnenolon wirkt außerdem als Botenstoff im Gehirn. Es ist zum Beispiel wichtig für das Gedächtnis, das Lernen und die Stimmung. Daneben reguliert es das Immunsystem.
Besteht ein Verdacht auf Nebennierenschwäche, wird der Arzt auf verschiedene Hormone testen (Bluttest wie: Cortisol, adrenocorticotropes Hormon (ACTH)).
Info
Unterschied zwischen Nebennierenschwäche und Nebenniereninsuffizienz: Bei der Nebennierenschwäche bleibt eine Restfunktion, bei einer Nebenniereninsuffizienz stellt die Nebenniere ihre Funktion vollständig ein. Die klassische Medizin behandelt nur eine Nebenniereninsuffizienz.
Eine Nebenniereninsuffizienz entsteht zum Beispiel als Folge einer Autoimmunerkrankung (Morbus Addison). Hier wird die Nebenniere vom Immunsystem zerstört, was unter Umständen lebensbedrohlich ist. Der Körper kann dann auf Belastung nicht reagieren: Wenn die Niere zum Beispiel morgens kein Cortisol ausschüttet, kann der Körper nicht vom Schlaf auf die Tagesaktivität umschalten.
Wie entsteht eine Nebennierenschwäche?
Über die Ursachen der Nebennierenschwäche wird noch diskutiert. Mediziner vermuten, dass eine chronische Stressbelastung die Nebennieren auf Dauer zu stark beansprucht und es so möglicherweise zu Ermüdungszuständen der Nebennieren kommt. Eine Schwächung könnte auch beim Burn-out-Syndrom oder bei chronischer Müdigkeit (CFS) der Fall sein. Zudem strapazieren seelische Krisen, wenig Schlaf oder Drogenmissbrauch die Nebennieren.
Auch eine schwache Entwicklung der Nebennieren oder zunehmendes Alter werden als Ursachen diskutiert. Daneben kann eine Nebennierenschwäche einer Autoimmunerkrankung wie Lupus erythematosus folgen, wenn der Körper die Drüsen angreift (autoimmune Nebennierenschwäche). Als Ursachen werden außerdem chronische Entzündungen oder eine gestörte Darmflora (Dysbiose) diskutiert. Auch bei einer Behandlung mit Kortison kann eine Nebennierenschwäche folgen. Diskutiert wird auch ein Zusammenhang mit dem chronischen Erschöpfungssyndrom (CFS).
Woran Sie eine Nebennierenschwäche erkennen
Bei schwacher Nebennierenfunktion reagiert der Körper auf alle körperlichen und seelischen Anstrengungen wie Kälte, Hunger, Unterzuckerung, Gifte oder Krankheiten zu schwach. Typische Symptome bei Nebennierenschwäche sind daher Gewichtsverlust, Müdigkeit, Schwindel und Schwächezustände. Selbst das morgendliche Aufstehen wird zum Problem.
Andere Beschwerden können folgen wie geringe Stressresistenz und Aufmerksamkeit, Konzentrationsstörungen und Antriebslosigkeit, Depressionen, Unruhe bis hin zu Panikattacken, Schlafstörungen, Darmflorastörungen und Verdauungsstörungen (Bauchschmerzen, Durchfall, Übelkeit), sexuelle Lustlosigkeit und erhöhte Infektanfälligkeit. Es wird vermutet, dass durch diese Umstände vermehrt Erkrankungen wie Diabetes, Herzerkrankungen und Krebs ausgelöst werden.
Einen anerkannten Test auf Nebennierenschwäche gibt es noch nicht. Der Arzt kann eine Nebennierenschwäche an den unklaren Symptomen auch nur schwer erkennen. Es gibt aber die Möglichkeit, verschiedene Hormone sowie den täglichen Cortisolverlauf zu messen. Am Morgen sollte der Cortisolspiegel erhöht sein, im Verlauf des Tages sinkt er. Wenn die morgendliche Erhöhung zu schwach ausfällt, könnte eine Nebennierenschwäche vorliegen. Übrigens: Wenn sich eine Nebennierenschwäche entwickelt, wird vorübergehend zu viel Cortisol festgestellt, erst am Ende des Krankheitsverlaufs zu wenig.
Expertenwissen
Nebenniere und Schilddrüse beeinflussen sich gegenseitig. Manchmal kann es so aussehen, als ob nur ein Organ für die Hormonstörung verantwortlich ist. Untersucht werden sollten daher die Hormone beider Organe. Auch ein Test auf entsprechende Autoantikörper ist ratsam. Im Zuge eines polyglandulären Syndroms kann es zudem zu einem Angriff auf Nebenniere und Schilddrüse (Hashimoto-Thyreoiditis, Morbus Basedow) kommen.
Die einfachste Behandlung kann manchmal darin bestehen, den aktuellen Stress auszuschalten und die natürliche Regulation wieder zu ermöglichen. Die Maßnahmen richten sich nach dem Patienten – zum Beispiel die Behandlung einer Schilddrüsenunterfunktion, eine Darmsanierung oder der Ausgleich eines Mikronährstoffmangels.
Ziele der Behandlung
Wie wird die Nebennierenschwäche klassisch behandelt und welcher Arzt ist Experte dafür?
Da die Nebennierenschwäche keine anerkannte Erkrankung ist, gibt es auch keine Empfehlung für eine entsprechende Therapie. So geht es im Grunde darum, Stress zu erkennen und zu reduzieren. Man braucht Gelegenheiten zur Erholung und sollte den Körper optimal ernähren und versorgen.
Für Hormonstörungen ist der Endokrinologe zuständig. Eine Nebennierenschwäche wird aber nur in der Mikronährstoffmedizin oder der Naturheilkunde behandelt. Da bei einer Nebennierenschwäche keine Gewebe zerstört werden, gilt sie als heilbar.
Info
Bei einer Nebenniereninsuffizienz müssen dagegen die fehlenden Hormone durch Medikamente ergänzt werden: Es gibt sogenannte Glukokortikoide, um den Mangel von körpereigenem Cortisol auszugleichen. Bei einem Mangel an Aldosteron verordnen Ärzte Fludrocortison. Ein DHEA-Mangel muss nicht zwingend ausgeglichen werden.
Ziele der Mikronährstoffmedizin
Die Mikronährstoffmedizin verfolgt mit einer Nahrungsergänzung drei Strategien: erstens den Stress zu reduzieren, zweitens die Stressfolgen abzumildern und drittens die Nebenniere zu stärken, sodass sie wieder Stresshormone produzieren kann. Denn Stresshormone braucht der Körper, um auf alltägliche Situationen zu reagieren. Folgende Nährstoffe sind dabei empfehlenswert:
- B-Vitamine als Nervennahrung
- Vitamin C zur Reduzierung der Stressantwort
- Vitamin D zur Stabilisierung der Stimmung
- Magnesium gegen die Stressfolgen
- Omega-3-Fettsäuren zum Schutz der Nervenzellen
- 5-Hydroxytryptophan und Tyrosin für die Bildung von Hormonen
- Gamma-Aminobuttersäure (GABA) zur Beruhigung und für einen guten Schlaf
- Theanin zur Entspannung
- Rosenwurz für eine bessere Stressresistenz
Am besten lässt man sich von einem Arzt oder Mikronährstoff-Experten beraten, der sich speziell mit Hormonen beschäftigt (Endokrinologe).
Info
Im Internet werden manchmal Mikronährstoffpräparate angeboten, die verschreibungspflichtige Hormone enthalten wie Cortisol, Thyroxin oder Progesteron. Wahrscheinlich gelangen diese Substanzen bei der Herstellung als Verunreinigung in die Präparate. Solche Hormone gehören nur in die Hand des Fachmanns. Man sollte daher beim Kauf unbedingt darauf achten, dass die Produkte aus einer vertrauenswürdigen Quelle stammen – vorzugsweise aus Deutschland oder aus Europa und von Herstellern, die ihre Präparate regelmäßigen Kontrollen unterziehen.
Behandlung mit Mikronährstoffen
B-Vitamine als Nervennahrung bei Stress
Wirkweise von B-Vitaminen
B-Vitamine sind für den gesamten Stoffwechsel inklusive der Produktion von Nervenbotenstoffen wichtig. Sie können in stressigen Situationen und bei Nebennierenschwäche unterstützend wirken. Wichtig sind vor allem:
- Pantothensäure (Vitamin B5): Erste Untersuchungen zeigen, dass die Nebenniere Pantothensäure braucht, um das Stresshormon Cortisol zu bilden. Ein Mangel kann Funktion und Gewebe der Nebenniere schwächen. Bei Stress sorgt Pantothensäure dafür, dass Cortisol vermehrt, aber nicht im Übermaß ausgeschüttet wird.
- Vitamin B6 und Folsäure: Vitamin B6 ist wichtig für Reaktionen, die die Nebenniere im Gehirn auslöst. Der Körper braucht es für die Herstellung von Nervenbotenstoffen mit beruhigender (wie GABA), aktivierender (wie Dopamin) und stimmungsaufhellender Funktion (wie Serotonin). Ähnlich wirkt Folsäure. Sie ist aber nur indirekt beteiligt.
- Niacin (Vitamin B3): Niacin ist das Vitamin für den Energiestoffwechsel und die Regeneration des Gewebes. Es unterstützt die Herstellung von Cortisol und Aldosteron (Salzhaushalt) sowie Serotonin (Stimmung).
- Vitamin B1: Erste Studien zeigen, dass Vitamin B1 Stressreaktionen entgegenwirken kann: Die Injektion in den Muskel vor einer Operation senkte die Cortisolwerte. Operationen bedeuten für den Körper immer Stress. Dabei steigt die Ausschüttung von Cortisol.
- Vitamin B12: In stressigen Phasen könnte Vitamin B12 dazu beitragen, die natürliche (vom Tag-Nacht-Rhythmus gesteuerte) Hormonproduktion zu normalisieren. Das führt dazu, dass man morgens leichter aktiv wird.
Forscher kommen zu dem Ergebnis, dass B-Vitamine Stresssymptome reduzieren können: Teilnehmer einer kleinen hochwertigen Studie litten an weniger Stresssymptomen, nachdem sie über vier Wochen ein Präparat mit hoch dosierten B-Vitaminen, Zink und Magnesium eingenommen hatten.
Auch bei chronischem Stress dürften hoch dosierte B-Vitamine eine stressreduzierende Wirkung haben. Erste Untersuchungen zeigen sogar, dass sie die natürliche im Tagesverlauf schwankende Cortisolausschüttung normalisierten. Der Körper kann so möglicherweise wieder mit alltäglichen Belastungen umgehen. Eine Übersichtsarbeit deutet an, dass besonders Menschen mit viel Stress und ungesunder Ernährung von B-Vitaminen profitieren könnten. Kombinationspräparate mit Mineralstoffen wirkten deutlich besser.
Fazit: Bei Nebennierenschwäche sind B-Vitamine bisher zwar nicht direkt getestet, zu Stress liegen jedoch erfolgreiche Studien vor. An der Wiederherstellung der Regulation sind viele Mikronährstoffe beteiligt. Daher wirken Kombinationspräparate wahrscheinlich besser.
Dosierung und Einnahmeempfehlung von B-Vitaminen
Zur Unterstützung der Nebennieren sind Multivitaminpräparate geeignet, die alle B-Vitamine in einer abgestimmten Dosierung enthalten: 5 bis 10 Milligramm der Vitamine B1, B2 und B6, 15 bis 25 Mikrogramm Vitamin B12, 200 bis 400 Mikrogramm Folsäure, 50 bis 100 Milligramm Niacin als Nicotinamid und 150 bis 200 Milligramm Pantothensäure.
Tipp
Bei der Wahl des Präparats sollten Sie darauf achten, dass es Folsäure in Form von 5-Methyltetrahydrofolat (5-MTHF) enthält. Dies ist die für den Körper sofort verwertbare Form von Folsäure.
Homocysteinspiegel im Labor bestimmen lassen
Bei anhaltendem Stress und Müdigkeit ist es sinnvoll, Homocystein im Blut überprüfen zu lassen. Homocystein ist ein indirektes Maß für die Versorgung mit B-Vitaminen. B-Vitamine werden für den Abbau von Homocystein gebraucht. Normale Werte für Homocystein im Blutplasma liegen unter 10 Mikromol pro Liter. Das Plasma ist der flüssige Teil des Blutes ohne Blutzellen.
B-Vitamine: zu beachten in der Schwangerschaft und Stillzeit, bei Erkrankungen und Medikamenteneinnahme
Schwangere und stillende Frauen sollten hoch dosierte Vitamin-B-Präparate nur bei einer nachgewiesenen Unterversorgung und in Rücksprache mit ihrem Arzt einnehmen.
Nierenpatienten sollten Vitamin B12 in Form von Methylcobalamin einnehmen und nicht als Cyanocobalamin. Letzteres ist in hoher Dosierung für Nierenpatienten vermutlich schädlich.
Menschen mit schwerer Herz-Kreislauf-Schwäche, einem frischen Herzinfarkt, akuten Blutungen, Magengeschwüren und schweren Lebererkrankungen sollten nicht mehr als 30 Milligramm Niacin täglich einnehmen.
Vitamin B6 kann ab einer Dosierung von über 5 Milligramm die Wirkung von Antiepileptika oder Parkinson-Medikamenten abschwächen. Das gilt für Phenobarbital (Luminal®) oder Phenytoin (Phenhydan®, Zentropil®) oder den Wirkstoff Levodopa (L-Dopa).
Folsäure könnte die Wirkung von Antibiotika mit den Wirkstoffen Trimethoprim (Infectotrimet®), Proguanil (Paludrine®) und Pyrimethamin (Daraprim®) vermindern.
Außerdem hemmt Niacin die Aufnahme bestimmter Antibiotika. Es sollte deshalb mit einem Abstand von zwei bis drei Stunden eingenommen werden. Dazu zählen Tetrazykline wie Fluorex Plus® oder Mysteclin®.
Vitamin C vermindert die Stressantwort
Wirkweise von Vitamin C

Die Nebenniere ist eines der Organe mit dem höchsten Gehalt an Vitamin C. Es hilft bei Herstellung von Hormonen und Nervenbotenstoffen, zum Beispiel des Stresshormons Noradrenalin. Noradrenalin hat aktivierende Wirkung und hilft, auf Stress zu reagieren. Bei Stress gibt die Nebenniere Vitamin C ins Blut ab. Dort bekämpft es oxidativen Stress, der bei Stressbelastungen entsteht. In stressigen Phasen ist der Bedarf deshalb erhöht.
Anfangsphase: Wenn die Nebenniere noch nicht erschöpft ist, sollte der Stress gesenkt werden. Erste Studien zeigen, dass die Einnahme von hoch dosiertem Vitamin C die Stressbelastung reduziert. Laut eines Übersichtsartikels senkt es bei Frauen auch den Blutdruck und Ängste. Zudem normalisierten sich die Cortisolwerte in einer hochwertigen Studie durch Vitamin C nach einer stressigen Situation schneller.
Spätphase: Selbst, wenn die Nebenniere erschöpft ist, könnte hoch dosiertes Vitamin C noch bei der Herstellung von Adrenalin und Noradrenalin helfen. Darauf deuten erste Studien bei Operationen oder einer Blutvergiftung (Sepsis) hin. Zudem könnte Vitamin C bei schweren Erkrankungen wie Krebs oder COVID-19 die starke Müdigkeit und Erschöpfung bekämpfen.
Fazit: Vitamin C hat eine große Bedeutung für die Nebenniere, denn ihr Vitamin-C-Gehalt ist hoch. Studien zu Nebennierenschwäche gibt es noch nicht. Es liegen jedoch schon viele Studien zur stress- und müdigkeitsdämpfenden Wirkung vor.
Dosierung und Einnahmeempfehlung von Vitamin C
Mikronährstoff-Experten empfehlen bei akutem körperlichem und seelischem Stress die Einnahme von täglich 1.000 bis 3.000 Milligramm Vitamin C für maximal eine Woche. Die Gesamtmenge sollte dabei auf den Tag verteilt werden (dreimal 1.000 Milligramm): Die Vitamin-C-Aufnahme im Darm nimmt mit steigender Dosierung ab.
Wird Vitamin C bei chronischem Stress über mehrere Wochen bis Monate hinweg eingenommen, ist eine Dosierung von 100 bis 200 Milligramm ratsam.
Vitamin C ist magenverträglicher, wenn man es zum Essen ergänzt. Für Personen mit empfindlichem Magen eignen sich zudem Präparate, die basisches Vitamin C enthalten wie Calciumascorbat. Es ist besser verträglich, da es Säure „abfängt“.
Vitamin C: zu beachten in der Schwangerschaft, bei Erkrankungen und Medikamenteneinnahme
In der Schwangerschaft wird eine Vitamin-C-Zufuhr von 110 Milligramm empfohlen. Für Stillende sind 150 Milligramm ratsam. Höhere Mengen sollte man mit dem Arzt absprechen. Bis 1.800 Milligramm pro Tag sind jedoch wahrscheinlich sicher.
Patienten mit Nierenschwäche (Niereninsuffizienz) sollten eine Einnahme von 500 Milligramm pro Tag nicht überschreiten. Bei Neigung zu Nierensteinen sollte die tägliche Dosis unter 1.000 Milligramm liegen.
Da Vitamin C die Eisenaufnahme verbessert, sollten bei Menschen mit einer Eisenspeicherkrankheit (Hämochromatose) höhere Vitamin-C-Gaben nur unter ärztlicher Aufsicht erfolgen.
Bei gleichzeitiger Einnahme bestimmter Medikamente und hoch dosiertem Vitamin C kann es in seltenen Fällen Wechselwirkungen geben: Ab 1.000 Milligramm sollte es nicht mit dem Blutgerinnungshemmer Warfarin (Coumadin®) kombiniert werden.
Auch könnte Vitamin C die Wirkung von Krebsmedikamenten hemmen, wie die des Blutkrebs-Medikaments Bortezomib (Velcade®) sowie von Doxorubicin (wie Adriblastin®, Ribodoxo®), Methotrexat (wie Bendatrexat®, Lantarel®) und Cisplatin (wie Cis-GRY®). Eine Vitamin-C-Ergänzung muss bei Krebs mit dem Arzt abgesprochen sein.
Vitamin-D-Mangel bei Nebennierenschwäche vermeiden
Wirkweise von Vitamin D
Vitamin D steuert viele Prozesse, so auch die Hormonproduktion. Es ist zum Beispiel an der Kommunikation von Gehirn und Nebenniere beteiligt (Hypothalamus-Hypophyse-Nebennieren-Achse). Ein Vitamin-D-Mangel könnte mit einer eingeschränkten Regulation des Stresshormons Cortisol und des Blutdruckhormons Aldosteron zusammenhängen. Daneben fördert Vitamin D die Produktion des Glücks- und Entspannungshormons Serotonin. Viele Menschen mit Nebenniereninsuffizienz haben einen schweren Mangel. Auch stehen niedrige Vitamin-D-Blutwerte mit Angstgefühlen, depressiver Verstimmung und Konzentrationsproblemen in Verbindung.
Wenn die Nebenniere vollständig ausfällt (Nebenniereninsuffizienz), droht auch eine Abwehrschwäche. Eine erste Studie mit Betroffenen zeigte, dass Vitamin D die Zahl bestimmter Abwehrzellen erhöhte.
Ein Angriff des Gewebes der Nebennieren (Autoimmunerkrankung) hängt offensichtlich auch mit niedrigen Vitamin-D-Spiegeln zusammen. Das zeigt eine große Beobachtungsstudie. Zudem zeigt eine erste Studie zur Vitamin-D-Einnahme günstige Effekte bei Menschen mit familiär gehäuften Autoimmunerkrankungen, die das Hormonsystem betreffen.
Fazit: Vitamin D ist bei einer Nebennierenschwäche noch nicht direkt getestet. Zu Depressionen und Abwehrschwäche liegen aber Studien vor. Ein Mangel ist in unseren Breitengraden häufig – vor allem im Winter. Bei einer Nebennierenschwäche sollte der Vitamin-D-Mangel ausgeglichen werden.
Vitamin D: Dosierung und Einnahmeempfehlung
Mikronährstoff-Experten empfehlen bei einer Nebennierenschwäche die tägliche Einnahme von 1.000 bis 2.000 Internationalen Einheiten Vitamin D. Dies sind allerdings nur Richtwerte. Im Idealfall wird die Dosierung individuell vom Arzt oder Mikronährstoff-Experten an die Versorgung angepasst. Bei einem Vitamin-D-Mangel sind meist für einige Wochen höhere Dosierungen nötig.
Da Vitamin D ein fettlösliches Vitamin ist, sollte es zum Essen eingenommen werden – so wird die Aufnahme im Darm unterstützt.
Vitamin D im Labor bestimmen lassen
Den Vitamin-D-Spiegel sollte man bestenfalls zweimal im Jahr kontrollieren lassen, zum Beispiel im Frühling und Herbst. Hierfür wird im Labor die Transportform 25(OH)-Vitamin D (Calcidiol) bestimmt. Optimalerweise liegt der Vitamin-D-Spiegel zwischen 40 und 60 Nanogramm pro Milliliter Blutserum. Das Blutserum ist der flüssige Teil des Blutes ohne Zellen und ohne Gerinnungsfaktoren.
Vitamin D: zu beachten bei Erkrankungen und Medikamenteneinnahme
Personen mit Nierenerkrankungen sollten Vitamin D nicht ohne Rücksprache mit dem Arzt einnehmen: Das Blut kann einen hohen Calciumspiegel aufweisen. Da Vitamin D die Calciumaufnahme im Darm steigert, können die Spiegel zu stark ansteigen. Auch Personen mit calciumhaltigen Nierensteinen sollten vorher mit dem Arzt sprechen.
Bei einigen Krankheiten ist ein gestörter Calcium- und Phosphatstoffwechsel möglich, zum Beispiel bei der Bindegewebserkrankung Sarkoidose sowie einer Nebenschilddrüsenüberfunktion. Betroffene sollten Vitamin D nicht ohne ärztliche Kontrolle einnehmen.
Entwässerungsmittel (Diuretika) aus der Gruppe der Thiazide senken die Ausscheidung von Calcium – der Calciumspiegel im Blut ist erhöht. Da auch Vitamin D den Calciumspiegel hochtreibt, darf Vitamin D nur mit Thiaziden eingenommen werden, wenn der Calciumspiegel regelmäßig überprüft wird. Dies betrifft die Wirkstoffe Hydrochlorothiazid (Esidrix®), Xipamid (Aquaphor®) und Indapamid (Natrilix®).
Magnesium hemmt die Ausschüttung von Stresshormonen
Wirkweise von Magnesium
Magnesium hat auf das Nervensystem vor allem beruhigende Wirkungen: Erste Studien liefern Hinweise darauf, dass es die Ausschüttung der Stresshormone Adrenalin und Noradrenalin aus der Nebenniere vermindert. Magnesium dämpft so nicht nur die unbewussten Stressfolgen (wie Herzschlag, Blutdruck und Muskelspannung), es nimmt auch Einfluss auf die seelische Stressreaktion.
Dauerhafter Stress führt zu einem Teufelskreis: Einerseits wird Magnesium freigesetzt, um auf den Reiz zu reagieren; andererseits wird dem Körper auf Dauer Magnesium entzogen. Daher ist der Magnesiumbedarf bei Stress erhöht.
Erste Studien zeigen einen Nutzen von Magnesium auf Stressfolgen wie Bluthochdruck, Schlafstörungen, Ängstlichkeit, Depressionen und Burn-out. Zu Nebennierenschwäche gibt es derzeit nur theoretische Hinweise. Da Magnesium gut verträglich ist, ist eine Ergänzung einen Versuch wert.
Dosierung und Einnahmeempfehlung von Magnesium
Bei Stress, Schlafstörungen und Depressionen empfehlen Mikronährstoff-Experten, täglich 300 bis 600 Milligramm Magnesium unterstützend einzunehmen. Langfristig sollte eine Einnahme von über 250 Milligramm pro Tag allerdings nicht ohne Laborkontrolle oder ärztliche Rücksprache erfolgen.
Sinnvoll ist die Einnahme zu den Mahlzeiten. Dadurch verbessert sich die Verträglichkeit. Ab 250 Milligramm kann es bei empfindlichen Menschen zu Durchfall kommen. Dann sollte die Menge auf mehrere Portionen aufgeteilt werden. So können Sie harmlosen Magen-Darm-Beschwerden vorbeugen, die bei Einnahme hoher Magnesiumdosen aufkommen können.
Magnesiumspiegel im Labor bestimmen lassen
Um einen Magnesiummangel festzustellen, wird im Labor der Spiegel im Vollblut bestimmt. Der normale Magnesiumwert im Vollblut liegt zwischen 1,38 und 1,50 Millimol pro Liter. Auch bei einer langfristigen Einnahme über 250 Milligramm Magnesium pro Tag ist die Bestimmung ratsam.
Magnesium: zu beachten bei Nierenerkrankungen und Medikamenteneinnahme
Magnesiumpräparate dürfen bei Nierenerkrankungen nur in Rücksprache mit dem Arzt eingenommen werden: Es kann eine Über- oder Unterversorgung vorliegen.
Bei einigen Antibiotika (zum Beispiel Gyrasehemmer wie Ciprofloxacin (Ciloxan®) und Tetrazykline wie Tetracyclin (Achromycin®)) sowie Osteoporose-Medikamenten (zum Beispiel Bisphosphonate wie Alendronat (Fosamax®, Tevanate®)) gibt es Einschränkungen für die Einnahme von Magnesium: Werden diese Medikamente eingenommen, sollten Sie einen Abstand von mindestens zwei Stunden zwischen dem Medikament und Magnesium einhalten.
Omega-3-Fettsäuren: Unterstützer in stressigen Phasen
Wirkweise von Omega-3-Fettsäuren
Omega-3-Fettsäuren werden für das Wachstum, die Reparatur, den Erhalt und den Schutz von Nervenzellen benötigt. Besonders wichtig sind Eicosapentaensäure (EPA) und Docosahexaensäure (DHA). Auch wirken sie auf die Stimmung und lindern Depressionen. Möglich sind eine geringere Stressantwort und ein geringeres Stressempfinden, wenn die Fettsäuren ergänzt werden.
Eine hochwertige Studie zeigt: Bei einer Alkoholentwöhnung kann die Einnahme von Omega-3-Fettsäuren die Cortisolausschüttung reduzieren und damit Stresssymptome mildern. Auch weitere kleinere Untersuchungen liefern erste Hinweise, dass Omega-3-Fettsäuren die körperlichen Folgen (Blutdruck, Energieverbrauch, Stresshormone) nach psychischem Stress hemmen können. Ein ähnlicher Effekt ließ sich bei schwangeren Frauen beobachten: Nach Einnahme von 450 Milligramm DHA fühlten sich die Frauen resistenter gegen Stress und schütteten weniger Stresshormone aus.
Dosierung und Einnahmeempfehlung von Omega-3-Fettsäuren
Mikronährstoff-Experten empfehlen bei Nebennierenschwäche versuchsweise täglich 1.500 bis 2.000 Milligramm Omega-3-Fettsäuren aus Fischöl, da dies reich ist an EPA und DHA. Vor allem EPA kann sich mit seinen entzündungshemmenden Eigenschaften positiv auf die Stimmung auswirken, zum Beispiel bei Depressionen. Diese Dosierung wurde in Studien bei Stress und Depressionen eingesetzt.
Omega-3-Präparate sollten zum Essen eingenommen werden: Zusammen mit Fett aus der Mahlzeit gelangen sie besser aus dem Darm in das Blut.
Tipp
Bei Omega-3-Fettsäuren aus Fischöl sollten Sie zu einem qualitativ hochwertigen Produkt greifen. Diese sollten speziell gereinigt sein, sodass sie frei von Rückständen und Schadstoffen sind. Personen, die auf tierische Produkte verzichten, etwa Veganer, können auf Algenöl zurückgreifen. Es ist zudem von Natur aus reiner, da die Algen unter kontrollierten Bedingungen angebaut werden.
Omega-3-Fettsäuren im Labor bestimmen lassen
Über den Omega-3-Index lässt sich nachweisen, ob ein Mangel an Omega-3-Fettsäuren vorliegt. Dazu wird beim Arzt ein Bluttest gemacht, bei dem der Anteil von EPA und DHA in den roten Blutkörperchen bestimmt wird.
Der Omega-3-Index wird in Prozent angegeben. Als optimal gilt ein Wert von 8 bis 11 Prozent. Dann sind acht bis elf von 100 Fettsäuren in den roten Blutkörperchen wertvolle Omega-3-Fettsäuren.
Omega-3-Fettsäuren: zu beachten bei Erkrankungen, Operationen und Einnahme von Blutverdünnern
Bei einer Lebererkrankung sowie einer akuten Bauchspeicheldrüsen- oder Gallenblasenentzündung sollten Omega-3-Fettsäuren nicht eingenommen werden.
Möglicherweise senken Omega-3-Fettsäuren den Blutzucker. Daher sollten Diabetiker, die Medikamente einnehmen, ihre Blutzuckerwerte zu Beginn der Einnahme häufiger kontrollieren. Eventuell ist eine Anpassung der Medikamente nötig, um eine Unterzuckerung zu vermeiden.
Bestimmte Herzrhythmusstörungen (Vorhofflimmern) könnten bei Vorerkrankungen häufiger auftreten, wenn mehr als 1.000 Milligramm Omega-3-Fettsäuren pro Tag eingesetzt werden. Liegen Herzrhythmusstörungen vor, sollte die Einnahme mit dem Arzt oder Mikronährstoff-Experten besprochen werden. Er kann das Risiko abwägen und begleitend den Omega-3-Index kontrollieren.
Omega-3-Fettsäuren wirken hoch dosiert vermutlich blutverdünnend. Personen mit Blutgerinnungsstörungen sollten die Einnahme zuvor mit dem Arzt abklären. Gleiches gilt vor einer geplanten Operation: In einer Vorstudie stieg das Blutungsrisiko nicht (2.000 Milligramm). Bisher gibt es jedoch wenig Daten.
Dosen über 1.000 Milligramm Omega-3-Fettsäuren täglich könnten die Wirkung von Blutgerinnungshemmern verstärken. Der Arzt sollte zur Sicherheit die Gerinnungswerte kontrollieren und gegebenenfalls die Dosierung anpassen. Dazu zählen Cumarin-Derivate (wie Marcumar®), Acetylsalicylsäure (ASS, Aspirin®), Heparin (Clexane®) und neue orale Antikoagulanzien wie Apixaban (Eliquis®) und Rivaroxaban (Xarelto®).
5-Hydroxytryptophan und Tyrosin: Hormonvorstufen
Wirkweise von 5-Hydroxytryptophan und Tyrosin
Viele Botenstoffe werden aus Aminosäuren hergestellt. Tryptophan ist zum Beispiel die Vorstufe des Glückshormons Serotonin. Serotonin wird in der Nebenniere gespeichert. Dort reguliert es die Ausschüttung von Stresshormonen. Man vermutet, dass Serotonin die Hirn-Nebennieren-Achse aktiviert und dabei hilft, die Stresshormone wieder aufzufüllen. Grundstoff für diese Stresshormone ist Tyrosin. Aus ihm wird Adrenalin hergestellt, aber auch Dopamin und Thyroxin. Diese Hormone ermöglichen eine aktivierende Antwort auf Stress.
Würde man Tryptophan direkt einnehmen, würde es bereits im Körper zu anderen Substanzen umgesetzt. Darum empfehlen Mikronährstoff-Experten meist 5-Hydroxytryptophan (5-HTP) aus Griffonia. 5-HTP ist die direkte Vorstufe von Serotonin, welche ins Gehirn gelangen kann. Es könnte bei Stress helfen und die Stimmung stabilisieren. Vorstudien zeigen auch, dass 5-HTP bei Depressionen auf die Nebenniere stimulierend wirken könnte. Daneben steigert es den Blutdruck, der bei Nebennierenschwäche zu niedrig ist.
Info
Bei Depressionen kann die Hirn-Nebennieren-Achse gestört sein: Dann produziert sie nicht zu wenig, sondern zu viel Cortisol. Das Medikament Dexamethason kann die Produktion unterdrücken. Wird anschließend 5-HTP gegeben, produziert die Nebenniere wieder Cortisol. Die Forscher folgern daraus, dass 5-HTP an der Regulation der Nebenniere beteiligt ist und bei Nebennierenschwäche aktivierend wirken könnte.
Da Griffonia müde machen kann, könnte Tyrosin die bessere Wahl sein. Menschen mit chronischer Müdigkeit (CFS) haben niedrigere Tyrosinwerte. Laut einem Übersichtsartikel hilft Tyrosin vermutlich dabei, dass bei gestressten Personen die Leistung nicht abnimmt. Auch sank in einer hochwertigen Studie das Stressempfinden, wenn Teilnehmer Tyrosin mit anderen Mikronährstoffen (B-Vitamine und Mineralstoffe) einnahmen. Allerdings gibt es auch Studien ohne Effekt.
Fazit: 5-HTP und Tyrosin sind wichtige Hormonvorstufen. Studien zu Nebennierenschwäche fehlen jedoch. Vermutlich ist Tyrosin dann geeignet, wenn Müdigkeit und mangelnde Reaktion auf Stress im Vordergrund stehen. 5-HTP hilft eher zur Beruhigung und bei depressiven Gefühlen.
Dosierung und Einnahmeempfehlung von 5-Hydroxtryptophan und Tyrosin
Mikronährstoff-Experten empfehlen bei Stress 150 bis 300 Milligramm 5-HTP aus Griffonia pro Tag in zwei oder drei Einzeldosen. Die Dosis sollte man langsam steigern und zunächst mit 50 Milligramm beginnen. Die Einnahme erfolgt für drei Monate und sollte von einem Arzt begleitet werden. Griffonia wird am besten zwischen den Mahlzeiten eingenommen. Die Einnahme zum Essen verbessert die Verträglichkeit. Dann sollte die Mahlzeit jedoch eiweißarm sein – zum Beispiel ohne Fleisch, Hülsenfrüchte oder Milchprodukte.
Treten Beschwerden wie Müdigkeit auf, sollte ein Mikronährstoff-Experte eine andere Behandlung vorschlagen, zum Beispiel mit 500 bis 1.000 Milligramm Tyrosin pro Tag. Tyrosin sollte über den Tag verteilt und nicht mit weiteren Aminosäuren eingenommen werden, da sie sich gegenseitig bei der Aufnahme hemmen. Auch ein Abstand zu eiweißreichen Mahlzeiten ist sinnvoll – am besten eine halbe Stunde vor dem Essen.
Info
Da einige Präparate mit künstlichem 5-HTP in den 90er-Jahren Verunreinigungen enthielten, sollte man auf einen seriösen Anbieter achten. Am besten geeignet ist pflanzliches 5-HTP aus Griffonia. Ein Extrakt enthält genau definierte Mengen im Gegensatz zu Samenpulver.
Idealerweise wird Griffonia-Extrakt in Kombination mit Vitamin B6 eingenommen, um eine optimale Umwandlung von 5-HTP in Serotonin zu gewährleisten. Bei Schlafstörungen und Stress ist eine Kombination mit Magnesium sinnvoll, um die Wirksamkeit zu verbessern. Schlägt 5-HTP bei Schlafstörungen nicht an, kann auch in Rücksprache mit dem Experten das Schlafhormon Melatonin versucht werden.
5-Hydroxytryptophan und Tyrosin: zu beachten in der Schwangerschaft und Stillzeit, bei Erkrankungen und Medikamenteneinnahme
Zur Sicherheit von 5-HTP und Tyrosin in Schwangerschaft und Stillzeit liegen keine Studien vor. Daher ist es in dieser Zeit nicht geeignet.
Menschen mit Diabetes, Leberzirrhose und schweren Nierenerkrankungen sollten die Einnahme von 5-HTP und Tyrosin mit dem Arzt absprechen: Es könnte passieren, dass die Stoffe nicht richtig abgebaut oder ausgeschieden werden. Personen mit Magen-Darm-Entzündungen sollten besser keine Griffonia-Präparate einnehmen: 5-HTP könnte Entzündungen verstärken.
Zudem sollte die Einnahme von 5-HTP und Tyrosin bei Blutdruckproblemen mit dem Arzt abgeklärt werden. Beide Stoffe könnten den Blutdruck beeinflussen (senken oder steigern). Bei schwarzem Hautkrebs ist Tyrosin nicht geeignet: Es könnte die Erkrankung verschlimmern. Bei Schizophrenie und Migräne könnte Tyrosin die Symptome verstärken. Tyrosin fördert möglicherweise die Produktion von Schilddrüsenhormonen. Bei einer Schilddrüsenüberfunktion ist es daher ebenfalls nicht geeignet.
5-HTP darf nicht mit folgenden Medikamenten eingenommen werden:
- Antidepressiva aus der Gruppe der Serotonin-Wiederaufnahmehemmer wie Fluoxetin (Fluxet®, Fluxetin-CT®) und trizyklische Antidepressiva wie Clomipramin (Anafranil®) sowie tetrazyklische Antidepressiva wie Mirtazapin (Remergil®, Mirtagamma®)
- schmerzlindernde Opioide wie Tramadol (Tramadolor®) und Methadon (Methaddict®)
- Migränemittel aus der Klasse der Triptane wie Sumatriptan (Imigran®)
- Parkinson-Medikamente wie Carbidopa und L-Dopa (zum Beispiel Isicom®, LCE-ratio®, Nacom®)
Für die Einnahme von Tyrosin mit Medikamenten gilt außerdem:
- Tyrosin könnte die Aufnahme von Parkinsonmedikamenten mit dem Wirkstoff Levodopa (Madopar®, Levopar®) hemmen. Halten Sie einen Einnahmeabstand von zwei Stunden ein und sprechen Sie vorher mit Ihrem Arzt.
- Tyrosin ist Vorläufer von Schilddrüsenhormonen. Es könnte die Wirkung von Medikamenten mit Schilddrüsenhormonen erhöhen. Dazu zählt der Wirkstoff L-Thyroxin (wie Berlthyrox® oder Euthyrox®).
- Menschen, die Antidepressiva aus der Wirkstoffgruppe der Monoaminooxidase-Hemmer (MAO-Hemmer) einnehmen (Jatrosom®, Aurorix®), sollten Tyrosin nur in Rücksprache mit ihrem Arzt einnehmen.
Gamma-Aminobuttersäure: beruhigt bei Stress
Wirkweise von Gamma-Aminobuttersäure
Gamma-Aminobuttersäure (GABA) ist einer der wichtigsten Botenstoffe im Gehirn, die eine beruhigende und entspannende Wirkung auf die Muskulatur haben. Zudem reguliert GABA das Zusammenspiel zwischen dem Stresshormon Adrenalin und dem Glückshormon Serotonin. Serotonin verbessert die Stimmung und wirkt auch beruhigend. Viele Medikamente zielen auf den GABA-Stoffwechsel ab, um Angst- und Stresserkrankungen oder Depressionen zu behandeln. Chronischer Stress setzt die dämpfende Wirkung von GABA herab. Vermutlich ist die Fähigkeit, auf GABA zu reagieren, deshalb bei einer Nebennierenschwäche eingeschränkt.
Einige Vorstudien zeigen, dass die Einnahme von GABA, im Vergleich zu einem Scheinmedikament, die psychische Belastbarkeit verbessert. Größere Studien sind allerdings noch notwendig, um festzustellen, wie gut GABA bei Nebennierenschwäche hilft. Eine unterstützende Wirkung wird aber vermutet.
Dosierung und Einnahmeempfehlung von Gamma-Aminobuttersäure
In der Mikronährstoffmedizin werden bei starker psychischer Belastung oder Burn-out 100 bis 500 Milligramm GABA pro Tag empfohlen. Sinnvoll ist die Einnahme zwischen den Mahlzeiten, zum Beispiel eine Stunde vor dem Essen. So verbessern sich die Aufnahme im Darm und die Wirksamkeit. Beim Absetzen ist es ratsam, die Dosis langsam zu senken.
GABA sollte nicht mit Alkohol und anderen Suchtmitteln eingenommen werden. Akuter Alkoholkonsum verstärkt möglicherweise die Wirkung.
Info
Magnesium verbessert die entspannende Wirkung von GABA noch zusätzlich. Daher ist eine Kombination empfehlenswert.
GABA: zu beachten in der Schwangerschaft und Stillzeit, bei Erkrankungen sowie Medikamenteneinnahme
Schwangere und Stillende sollten GABA nicht einnehmen. Es gibt keine Daten zur Sicherheit.
GABA könnte bei chronisch-entzündlichen Darmerkrankungen in Einzelfällen die Entzündung verstärken. Daher sollte ein Arzt vor der Einnahme kontaktiert werden.
Diabetiker sollten bei einer Ergänzung von GABA ihre Blutzuckerspiegel engmaschig kontrollieren: Es könnte den Blutzucker senken. Gegebenenfalls ist eine Absprache mit dem Arzt oder Mikronährstoff-Experten nötig.
Bei einigen seltenen Erbkrankheiten ist der Stoffwechsel von GABA oder seinen Bausteinen Glutamin oder Glutamat gestört (Gamma-Aminobuttersäure-Transaminase- oder Succinat-Semialdehyd-Dehydrogenase-Mangel). Vor der Einnahme sollte ärztlicher Rat eingeholt werden.
Menschen mit einer Suchterkrankung können leicht von Medikamenten abhängig werden, die am GABA-Rezeptor wirken. Zu GABA selbst liegen diesbezüglich keine Untersuchungen vor. Zur Sicherheit sollten Betroffene jedoch auf GABA verzichten.
Wechselwirkungen zwischen GABA und Medikamenten sind möglich. Bei folgenden Arzneimitteln sollte vorher ein Arzt gefragt werden:
- Medikamente gegen Epilepsie können die natürliche GABA-Menge im Körper erhöhen. Dazu zählen zum Beispiel Gabapentin (wie Gabagamma®), Phenobarbital (wie Luminal®) und Valproinsäure (wie Convulex®).
- GABA könnte die Wirkung von Blutdrucksenkern verstärken. Dazu gehören beispielsweise Betablocker mit dem Wirkstoff Bisoprolol (wie Bisoprolol®, Concor®) oder ACE-Hemmer mit dem Wirkstoff Captopril (wie Lopirin Cor®, Tensobon®).
- GABA kann beruhigende Medikamente verstärken. Sie sollten nicht zusammen eingesetzt werden. Dazu zählen Benzodiazepine wie Clonazepam (Rivotril®), Midazolam (Dormicum®) oder auch Narkosemittel (Disoprivan®, Recofol®).
- Medikamente aus der Gruppe der Neurosteroide beeinflussen die Wirkung von GABA: Pregnenolon und Allopregnanolon/Brexanolon (Zulresso®) sowie Progesteron (wie Crinone®, Progestogel®) verstärken die GABA-Wirkung. Dehydroepiandrosteron (DHEA) (wie Intrarosa®) und seine Stoffwechselprodukte DHEA-Sulfat und Androsteron hemmen sie.
Theanin: beruhigender Inhaltsstoff aus Tee
Wirkweise von Theanin
Theanin ist eine Aminosäure, die hauptsächlich in grünem Tee enthalten ist. Sie hat eine entspannende und beruhigende Wirkung, wie auch verschiedene vorläufige Studien belegen: Studienteilnehmer, die Theanin einnahmen, hatten niedrigere Werte des Stresshormons Cortisol. Forscher vermuten, dass die Einnahme von Theanin die Stressantwort über die Nebenniere hemmen könnte. Der wahrgenommene Stress war bei den Teilnehmern der Studie eine Stunde nach der Theanineinnahme geringer als mit einem Scheinmedikament. Jedoch war der Effekt nach drei Stunden nicht mehr erkennbar.
Zwei weitere kleine vorläufige Studien zeigen, dass Theanin auch den Blutdruck bei gestressten Personen sowie depressive Beschwerden und Ängste bei Personen mit Depressionen senken konnte.
Dosierung und Einnahmeempfehlung von Theanin
Mikronährstoff-Experten empfehlen bei Stress die Einnahme von 200 bis 400 Milligramm Theanin pro Tag. Idealerweise sollte Theanin auf nüchternen Magen eingenommen werden, zum Beispiel eine Stunde vor dem Essen. Dies verbessert die Wirkung.
Theanin: zu beachten in der Schwangerschaft und Stillzeit, bei Erkrankungen und Medikamenteneinnahme
Zur Anwendung von Theanin in der Schwangerschaft und Stillzeit liegen keine ausreichenden Daten vor. Sicherheitshalber wird deshalb davon abgeraten.
Es gibt Hinweise darauf, dass Theanin den Blutdruck senken kann. Daher ist bei Menschen mit zu niedrigem Blutdruck Vorsicht geboten und eine Rücksprache mit dem Arzt sinnvoll. Bei einer Einnahme von Bluthochdruck-Medikamenten muss die Blutdruckeinstellung vor allem zu Beginn der Ergänzung regelmäßig überprüft werden. Sprechen Sie eine Einnahme ebenfalls mit Ihrem Arzt ab, wenn Sie unter Epilepsie leiden.
Theanin könnte die Wirkung von Alkohol und nervenwirksamen Medikamenten verstärken. Wenn Sie Medikamente gegen psychische Störungen oder Nervenerkrankungen einnehmen, sprechen Sie mit Ihrem Arzt. Das gilt vermutlich für Benzodiazepine (zum Beispiel Diazepam wie Valium® oder Bromazepam wie Lexotanil®), Barbiturate (zum Beispiel Phenobarbital wie Luminal®) und ähnliche.
Möglicherweise verstärkt Theanin die Wirkung bestimmter Krebsmedikamente mit den Wirkstoffen Doxorubicin und Andriamycin (wie Adriblastin®, Adrimedac®). Eine Einnahme sollte man mit dem Arzt besprechen.
Rosenwurz steigert die Stressresistenz
Wirkweise von Rosenwurz
In der traditionellen Medizin ist Rosenwurz als Adaptogen bekannt. Das ist ein Stoff, der dem Körper hilft, sich besser an stressige Situationen anzupassen. Die Inhaltstoffe (Rosavine) von Rosenwurz bremsen die Ausschüttung des Stresshormons Cortisol. Darüber hinaus wird eine antidepressive und angstlösende Wirkung vermutet.
In einer Vorstudie zeigten Forscher, dass Rosenwurz-Extrakt bereits nach drei Tagen Stresssymptome lindern konnte. Andere Wissenschaftler stellten in ihrer Vorstudie einen Rückgang von Stress, Ängsten, Wut, Verwirrtheit und Depressionen fest. Zudem könnte Rosenwurz geistige und körperliche Müdigkeit reduzieren. Bei Nebennierenschwäche wurde Rosenwurz noch nicht getestet. Die Ergänzung ist jedoch einen Versuch wert.
Info
Auch weitere Heilpflanzen könnten bei Nebennierenschwäche sinnvoll sein. Studien liegen für Ginseng, Taigawurzel und Süßholz vor. Die Pflanzen helfen dem Körper dabei, sich besser an Veränderungen anzupassen. Sie zählen ebenso zu den Adaptogenen. Führt Rosenwurz zu keiner Besserung, sind sie daher ebenfalls einen Versuch wert.
Dosierung und Einnahmeempfehlung von Rosenwurz
Für eine bessere Anpassung an stressige Situationen empfehlen Mikronährstoff-Experten täglich 100 bis 300 Milligramm Rosenwurz-Extrakt. Der Extrakt sollte auf einen Rosavingehalt von 1 bis 2 Prozent standardisiert sein. Umgerechnet sind dies bei 100 Milligramm Extrakt 1 bis 2 Milligramm Rosavine.
In Studien wurde Rosenwurz meist zwischen einem und zwei Monaten eingesetzt. Eine längere Einnahme sollte mit dem Arzt oder Mikronährstoff-Experten abgesprochen werden.
Rosenwurz: zu beachten in der Schwangerschaft und Stillzeit, bei Erkrankungen und Medikamenteneinnahme
Schwangere und Stillende sollten keine Präparate mit Rosenwurz einnehmen. Es gibt noch keine ausreichenden Daten zur Unbedenklichkeit.
Rosenwurz kann in der Leber Enzyme hemmen, die Medikamente abbauen. Dadurch ist es möglich, dass ein Extrakt den Abbau von bestimmten Medikamenten verlangsamt und deren Wirkung verstärkt. Sie sollten deshalb nicht zusammen mit Medikamenten eingenommen werden.
Personen, die Medikamente gegen Diabetes einnehmen, sollten ihren Blutzucker engmaschig überprüfen. Rosenwurz kann den Blutzucker senken und könnte eine Unterzuckerung auslösen.
Dosierungen auf einen Blick
Empfehlung pro Tag bei Nebennierenschwäche | |
|---|---|
Vitamine | |
Vitamin B1 | 5 bis 10 Milligramm (mg) |
Vitamin B2 | 5 bis 10 Milligramm |
Vitamin B6 | 5 bis 10 Milligramm |
Vitamin B12 | 15 bis 25 Mikrogramm (µg) |
Folsäure | 200 bis 400 Mikrogramm |
Niacin | 50 bis 100 Milligramm |
Pantothensäure | 150 bis 200 Milligramm |
Vitamin C | 1.000 bis 3.000 Milligramm |
Vitamin D | 1.000 bis 2.000 Internationale Einheiten (IE) |
Mineralstoffe | |
Magnesium | 300 bis 600 Milligramm |
Fettsäuren | |
Omega-3-Fettsäuren | 1.500 bis 2.000 Milligramm mit hohem DHA-Gehalt |
Aminosäuren | |
5-Hydroxytryptophan | 150 bis 300 Milligramm |
Tyrosin | 500 bis 1.000 Milligramm |
Gamma-Aminobuttersäure | 100 bis 500 Milligramm |
Theanin | 200 bis 400 Milligramm |
Pflanzenstoffe | |
Rosenwurz-Extrakt | 100 bis 300 Milligramm |
Sinnvolle Laboruntersuchungen auf einen Blick
Sinnvolle Blutuntersuchungen bei Nebennierenschwäche | |
|---|---|
Normalwerte | |
Homocystein (Plasma) | unter 10 Mikromol pro Liter (µmol/l) |
Vitamin D als 25(OH)-Vitamin D (Serum) | 40 bis 60 Nanogramm pro Milliliter (ng/ml) |
Magnesium (Vollblut) | 1,38 bis 1,50 Millimol pro Liter (mmol/l) |
Omega-3-Index (Erythrozyten) | 5 bis 8 Prozent (%) |
Zusammenfassung
Bei Stress sowie andauernder körperlicher und mentaler Belastung löst der Körper eine Stressantwort aus: Die Nebennieren schütten Stresshormone wie Cortisol aus und setzen andere ausgleichende Prozesse in Gang. Es wird vermutet, dass eine andauernde Belastung zu einer Erschöpfung der Nebenniere führt und damit zu einer Nebennierenschwäche.
Die Mikronährstoffmedizin kann bei einer Nebennierenschwäche unterstützen: B-Vitamine wie Pantothensäure, Niacin, Vitamin B1, B6, B12 und Folsäure dienen als Nervennahrung und optimieren den Stoffwechsel sowie die Energieproduktion. Omega-3-Fettsäuren aus Fischöl, Vitamin C, Vitamin D und Magnesium können helfen, die Stressantwort des Körpers zu reduzieren und die seelische Befindlichkeit zu stabilisieren.
Auch die Aminosäuren 5-Hydroxytryptophan, GABA sowie Theanin aus grünem Tee tragen zum seelischen Wohlbefinden und zur Entspannung bei. Rosenwurz und Tyrosin helfen vermutlich dabei, sich an stressige Situationen besser anzupassen.
Verzeichnis der Studien und Quellen
Aghajafari, F. et al. (2018): Vitamin D Deficiency and Antenatal and Postpartum Depression: A Systematic Review. Nutrients 2018 Apr 12;10(4):478. https://pubmed.ncbi.nlm.nih.gov/29649128/, abgerufen am: 23.06.2021.
Akturk, H. K. et al. (2018): Over-the-Counter “Adrenal Support” Supplements Contain Thyroid and Steroid-Based Adrenal Hormones. Mayo Clinic Proceedings 2018 Mar 1;93(3). https://www.mayoclinicproceedings.org/article/S0025-6196(17)30835-2/fulltext, abgerufen am: 10.08.2022.
Altieri, B. et al. (2017): Does vitamin D play a role in autoimmune endocrine disorders? A proof of concept. Rev Endocr Metab Disord 2017 Sep;18(3):335-46. https://pubmed.ncbi.nlm.nih.gov/28070798/, abgerufen am: 09.08.2022.
Akturk, H.K. et al. (2018): Over-the-Counter "Adrenal Support" Supplements Contain Thyroid and Steroid-Based Adrenal Hormones. Mayo Clin Proc. 2018 Mar;93(3):284-290. https://pubmed.ncbi.nlm.nih.gov/29502560/
Anderson, E. W. et al. (2021): Quinolinic acid, a kynurenine/tryptophan pathway metabolite, associates with impaired cognitive test performance in systemic lupus erythematosus. Lupus Sci Med 2021 Oct;8(1):e000559. https://pubmed.ncbi.nlm.nih.gov/34686589/, abgerufen am: 10.08.2022.
Anghelescu, I.-G. et al. (2018): Stress Management and the Role of Rhodiola rosea: A Review. Int J Psychiatry Clin Pract. 2018 Nov;22(4):242-252. https://pubmed.ncbi.nlm.nih.gov/29325481/, abgerufen am: 31.05.2021.
Armando, I. et al. (2003): The serotonin transporter is required for stress-evoked increases in adrenal catecholamine synthesis and angiotensin II AT(2) receptor expression. Neuroendocrinology 2003 Oct;78(4):217-25. https://pubmed.ncbi.nlm.nih.gov/14583654/, abgerufen am: 09.08.2022.
Armborst, D. et al. (2018): Impact of a Specific Amino Acid Composition with Micronutrients on Well-Being in Subjects with Chronic Psychological Stress and Exhaustion Conditions: A Pilot Study. Nutrients 2018 Apr 29;10(5):551. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5986431/, abgerufen am: 10.08.2022.
Armborst, D. et al. (2018): Impact of a Specific Amino Acid Composition with Micronutrients on Well-Being in Subjects with Chronic Psychological Stress and Exhaustion Conditions: A Pilot Study. Nutrients 2018;10(5):551. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5986431/, abgerufen am: 10.08.2022.
Auxtero, M.D. et al. (2021): Potential Herb-Drug Interactions in the Management of Age-Related Cognitive Dysfunction. Pharmaceutics 2021;13(1):124. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7835864/, abgerufen am: 28.06.2021.
Barbadoro, P. et al. (2013): Fish oil supplementation reduces cortisol basal levels and perceived stress: a randomized, placebo-controlled trial in abstinent alcohilics. Mol Nutr Food Res 2013 Jun;57(6):1110-4. https://www.ncbi.nlm.nih.gov/pubmed/23390041, abgerufen am: 06.09.2018.
Bargujar, P. et al. (2021): A Perplexing Presentation of SLE as Adrenal Insufficiency in a Young Male. Indian Journal of Endocrinology and Metabolism 2021 Jan-Feb;25(1):69-72. https://journals.lww.com/indjem/Fulltext/2021/01000/A_Perplexing_Presentation_of_SLE_as_Adrenal.15.aspx, abgerufen am: 09.08.2022.
Bellan, M. et al. (2020): Pathophysiological Role and Therapeutic Implications of Vitamin D in Autoimmunity: Focus on Chronic Autoimmune Diseases. Nutrients 2020 Mar 17;12(3):789. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7146294/, abgerufen am: 10.08.2022.
Benedictine University (2014): Clinical Trial: Effects of Exercise and 5-HTP on Cortisol Levels. clinicaltrials.gov/ct2/show/study/NCT02187341 , abgerufen am: 09.08.2022.
Bengtsson, A. A. et al. (2016): Metabolic Profiling of Systemic Lupus Erythematosus and Comparison with Primary Sjögren's Syndrome and Systemic Sclerosis. PLoS One 2016 Jul 21;11(7):e0159384. https://pubmed.ncbi.nlm.nih.gov/27441838/, abgerufen am: 09.08.2022.
Bertone-Johnson, E.R. (2009): Vitamin D and the occurrence of depression: causal association or circumstantial evidence? Nutr Rev 2009 Aug;67(8):481-92. https://pubmed.ncbi.nlm.nih.gov/19674344/, abgerufen am: 16.06.2021.
Bertone-Johnson, E. R. (2009): Vitamin D and the occurrence of depression: causal association or circumstantial evidence?. Nutr Rev 2009;67(8):481-92. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2950608/, abgerufen am: 10.08.2022.
Bhat, R. et al. (2014): Systemic lupus erythematosus presenting as acute adrenal insufficiency: a rare clinical presentation. Ann Med Health Sci Res 2014;4(1):140-2. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3952287/, abgerufen am: 10.08.2022.
Biesalski, H. K. et al. (2010): Ernährungsmedizin. 4. Aufl. Georg Thieme Verlag Stuttgart.
Biesalski, H. K. (2016): Vitamine und Minerale. Indikation, Diagnostik, Therapie. Georg Thieme Verlag Stuttgart.
Blankfield, A. (2013): Kynurenine Pathway Pathologies: do Nicotinamide and Other Pathway Co-Factors have a Therapeutic Role in Reduction of Symptom Severity, Including Chronic Fatigue Syndrome (CFS) and Fibromyalgia (FM). Int J Tryptophan Res 2013 Jul 21;6(Suppl 1):39-45. https://pubmed.ncbi.nlm.nih.gov/23922501/, abgerufen am: 16.06.2021.
Boyle, N.B. et al. (2017): The Effects of Magnesium Supplementation on Subjective Anxiety and Stress-A Systematic Review Nutrients 2017 May;9(5):429. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5452159/, abgerufen am 22.10.2018.
Brindley, R. L. et al. (2017): Serotonin and Serotonin Transporters in the Adrenal Medulla: A Potential Hub for Modulation of the Sympathetic Stress Response. ACS Chem Neurosci 2017 May 17;8(5):943-54. https://pubmed.ncbi.nlm.nih.gov/28406285/, abgerufen am: 09.08.2022.
Brindley, R. L. et al. (2019): Adrenal serotonin derives from accumulation by the antidepressant-sensitive serotonin transporter. Pharmacol Res 2019;140:56-66. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6286867/, abgerufen am: 10.08.2022.
Brody, S. et al. (2002): A randomized controlled trial of high dose ascorbic acid for reduction of blood pressure, cortisol, and subjective responses to psychological stress. Psychopharmacology (Berl) 2002 Jan;159(3):319-24. https://pubmed.ncbi.nlm.nih.gov/11862365/, abgerufen am: 10.08.2022.
Brown, J. et al. (2020): Intestinal Dysbiosis and Tryptophan Metabolism in Autoimmunity. Front Immunol 2020;11:1741. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7417361/, abgerufen am: 10.08.2020.
Bundesinstitut für Risikobewertung (BfR) (2012): Risikobewertung von Pflanzen und pflanzlichen Zubereitungen. https://www.bfr.bund.de/cm/350/risikobewertung-von-pflanzen-und-pflanzlichen-zubereitungen.pdf, abgerufen am: 28.06.2021.
Bundeszentrum für Ernährung (2020): Tee: Gesund trinken. Beliebtes Getränk mit gesundem Genuss. https://www.bzfe.de/inhalt/tee-gesund-trinken-28491.html, abgerufen am: 16.06.2021.
Burns, N. et al. (1996): The role of L-aromatic amino acid decarboxylase in serotonin-stimulated aldosterone secretion in response to salt intake. Endocr Res 1996 Nov;22(4):577-8. https://pubmed.ncbi.nlm.nih.gov/8969914/, abgerufen am: 28.06.2021.
Cadegiani, F.A. & Kater, C.E. (2016): Adrenal fatigue does not exist: a systematic review. BMC Endocr Disord 2016 Aug 24;16(1):48. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4997656/, abgerufen am: 31.08.2018.
Camfield, D.A. et al (2013): The effects of multivitamin supplementation on diurnal cortisol secretion and perceived stress. Nutrients 2013 Nov 11;5(11):4429-50. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3847740/, abgerufen am: 04.09.2018.
Carroll, D. et al. (2000): The effects of an oral multivitamin combination with calcium, magnesium, and zinc on psychological well-being in healthy young male volunteers: a double-blind placebo-controlled trial. Psychopharmacology (Berl) 2000 Jun;150(2):220-5. https://www.ncbi.nlm.nih.gov/pubmed/10907676/, abgerufen am: 04.09.2018.
Castell, L.M. et al. (1999): The role of tryptophan in fatigue in different conditions of stress. Adv Exp Med Biol 1999;467:697-704. https://pubmed.ncbi.nlm.nih.gov/10721121/, abgerufen am: 16.06.2021.
Cerit, H. et al. (2013): The effect of tryptophan on the cortisol response to social stress is modulated by the 5-HTTLPR genotype. Psychoneuroendocrinology 2013;38(2):201-208. https://www.sciencedirect.com/science/article/pii/S030645301200193X, abgerufen am: 07.09.2018.
Choi, S. C. et al. (2020): Gut microbiota dysbiosis and altered tryptophan catabolism contribute to autoimmunity in lupus-susceptible mice. Sci Transl Med 2020 Jul 8;12(551):eaax2220. https://pubmed.ncbi.nlm.nih.gov/32641487/, abgerufen am: 10.08.2022.
Choi, S. et al. (2011): Effect of chronic protein ingestion on tyrosine and tryptophan levels and catecholamine and serotonin synthesis in rat brain. Nutr Neurosci 2011 Nov;14(6):260-7. https://pubmed.ncbi.nlm.nih.gov/22053757/, abgerufen am: 09.08.2022.
Cowen, P. (2002). Cortisol, serotonin and depression: All stressed out? British Journal of Psychiatry 2002;180(2):99-100. https://www.cambridge.org/core/journals/the-british-journal-of-psychiatry/article/cortisol-serotonin-and-depression-all-stressed-out/766A58A46F537EA85FB5CB9AEDF33552, abgerufen am: 10.08.2022.
Cropley, M. et al. (2015): The Effects of Rhodiola Rosea L. Extract on Anxiety, Stress, Cognition and Other Mood Symptoms. Phytother Res. 2015 Dec;29(12):1934-9. https://pubmed.ncbi.nlm.nih.gov/26502953/, abgerufen am: 31.05.2021.
Cuciureanu, M. D. et al. (2011): Magnesium and stress. In: Magnesium in the Central Nervous System [Internet]. Adelaide (AU): University of Adelaide Press;2011. https://www.ncbi.nlm.nih.gov/books/NBK507250/, abgerufen am: 10.08.2022.
Danilenko, O.V. et al (2022): Chronic Fatigue Exhibits Heterogeneous Autoimmunity Characteristics Which Reflect Etiology. Pathophysiology. 2022 May 25;29(2):187-199. https://pubmed.ncbi.nlm.nih.gov/35736644/
Das, D. et al. (2016): Effect of Vitamin C on adrenal suppression by etomidate induction in patients undergoing cardiac surgery: A randomized controlled trial. Ann Card Anaesth 2016 Jul-Sep;19(3):410-7. https://pubmed.ncbi.nlm.nih.gov/27397444/, abgerufen am: 09.08.2022.
Das, Y. T. et al. (2004): Safety of 5-hydroxy-L-tryptophan. Toxicol Lett 2004 Apr 15;150(1):111-22. https://pubmed.ncbi.nlm.nih.gov/15068828/, abgerufen am: 09.08.2022.
De Koning, E.J. et al. (2015): Vitamin D supplementation to prevent depression and poor physical function in older adults: Study protocol of the D-Vitaal study, a randomized placebo-controlled clinical trial. BMC Geriatr 2015 Nov 19;15:151. https://pubmed.ncbi.nlm.nih.gov/26585952/, abgerufen am: 28.06.2021.
De Olivera, I.J. et al. (2015): Effects of Oral Vitamin C Supplementation on Anxiety in Students: A Double-Blind, Randomized, Placebo-Controlled Trial. Pak J Biol Sci 2015 Jan;18(1):11-8. https://www.ncbi.nlm.nih.gov/pubmed/26353411, abgerufen am: 05.09.2018.
Delarue, J. et al. (2003): Fish oil prevents the adrenal activation elicited by mental stress in healthy men. Diabetes Metab 2003 Jun;29(3):289-95. https://www.ncbi.nlm.nih.gov/pubmed/12909818, abgerufen am: 06.09.2018.
Deutsche Gesellschaft für Endokrinologie. Hormone und Stoffwechsel. Nebennierenhormonmangel – „Nebenniereninsuffizienz“. https://www.endokrinologie.net/krankheiten-nebenniereninsuffizienz.php, abgerufen am: 31.08.2018.
Duarte-Delgad, N. P. et al. (2022): Metabolites and metabolic pathways associated with rheumatoid arthritis and systemic lupus erythematosus. J Transl Autoimmun 2022;5:100150. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8897586/, abgerufen am: 10.08.2022.
Ebadi, M. (1981): Regulation and function of pyridoxal phosphate in CNS. Neurochem Int 1981;3(3-4):181-205. https://www.ncbi.nlm.nih.gov/pubmed/19643063, abgerufen am 04.09.2018.
Edwards, D. et al. (2012): Therapeutic Effects and Safety of Rhodiola Rosea Extract WS® 1375 in Subjects With Life-Stress Symptoms--Results of an Open-Label Study. Phytother Res. 2012 Aug;26(8):1220-5. https://pubmed.ncbi.nlm.nih.gov/22228617/, abgerufen am: 31.05.2021.
European Food Safety Authority (EFSA) (Hrsg) (2015): Scientific Opinion on Dietary Reference Values for magnesium. EFSA Journal 2015;13(7):4186. https://www.efsa.europa.eu/de/efsajournal/pub/4186, abgerufen am 31.01.2023
Feldhaus, S. (2018): Orthomolekulare Medizin bei Erschöpfung. Erfahrungsheilkunde (EHK) 2018;67:98–103. https://www.thieme-connect.com/products/ejournals/pdf/10.1055/a-0575-7805.pdf, abgerufen am: 28.06.2021.
Fernstrom, J. D. & Fernstrom, M. H. (2007): Tyrosine, phenylalanine, and catecholamine synthesis and function in the brain. J Nutr 2007 Jun;137(6 Suppl 1):1539S-1547S; discussion 1548S. https://pubmed.ncbi.nlm.nih.gov/17513421/, abgerufen am: 09.08.2022.
Fitzgerald, J.S. et al. (2018): Association between vitamin D status and testosterone and cortisol in ice hockey players. Biol Sport 2018;35(3):207-213. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6224848/, abgerufen am: 28.06.2021.
Freek, J.H. et al (2018): Hydrocortisone Affects Fatigue and Physical Functioning Through Metabolism of Tryptophan: A Randomized Controlled Trial. The Journal of Clinical Endocrinology & Metabolism 2018 Sep;103(9):3411-9. https://academic.oup.com/jcem/article/103/9/3411/5047295, abgerufen am: 16.06.2021.
Galușca, D. et al. (2022): Vitamin D Implications and Effect of Supplementation in Endocrine Disorders: Autoimmune Thyroid Disorders (Hashimoto's Disease and Grave's Disease), Diabetes Mellitus and Obesity. Medicina (Kaunas) 2022 Jan 27;58(2):194. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8877323/, abgerufen am: 10.08.2022.
Gartside, S.E. et al. (2010): The neurosteroid dehydroepiandrosterone (DHEA) and its metabolites alter 5-HT neuronal activity via modulation of GABAA receptors. J Psychopharmacol 2010 Nov;24(11):1717-24. https://pubmed.ncbi.nlm.nih.gov/19493957/, abgerufen am: 16.06.2021.
Georgiades, E. et al. (2003): Chronic fatigue syndrome: new evidence for a central fatigue disorder. Clin Sci (Lond) 2003 Aug;105(2):213-8. https://pubmed.ncbi.nlm.nih.gov/12708966/, abgerufen am: 09.08.2022.
Gröber, U. (2011): Mikronährstoffe. Metabolic Tuning – Prävention – Therapie. 3. Aufl. Wissenschaftliche Verlagsgesellschaft mbH Stuttgart.
Gröber, U. (2015): Interaktionen, Arzneimittel und Mikronährstoffe. 2. Aufl. Wissenschaftliche Verlagsgesellschaft Stuttgart.
Gröber, U. (2018): Arzneimittel und Mikronährstoffe – Medikationsorientierte Supplementierung. 4. Aufl. Wissenschaftliche Verlagsgesellschaft Stuttgart.
Hahn, J. et al. (2022): Vitamin D and marine omega 3 fatty acid supplementation and incident autoimmune disease: VITAL randomized controlled trial. BMJ 2022 Jan 26;376:e066452. https://pubmed.ncbi.nlm.nih.gov/35082139/, abgerufen am: 10.08.2022.
Hamazaki, T. et al. (2000): Anti-stress effects of DHA. Biofactors 2000;13(1-4):41-5. https://www.ncbi.nlm.nih.gov/pubmed/11237197, abgerufen am: 06.09.2018.
Hansen, A.L. et al. (2020): Vitamin D Supplementation during Winter: Effects on Stress Resilience in a Randomized Control Trial. Nutrients 2020;12(11):3258. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7692327/, abgerufen am: 28.06.2021.
Harada, K. et al. (2016): GABA Signaling and Neuroactive Steroids in Adrenal Medullary Chromaffin Cells. Front Cell Neurosci 2016 Apr 18;10:100. https://pubmed.ncbi.nlm.nih.gov/27147972/, abgerufen am: 09.08.2022.
Harada, K. et al. (2021): Mechanisms for establishment of GABA signaling in adrenal medullary chromaffin cells. J Neurochem 2021 Jul;158(2):153-68. https://pubmed.ncbi.nlm.nih.gov/33704788/, abgerufen am: 10.08.2022.
Haskell, C.F. et al. (2010): Effects of a multi-vitamin/mineral supplement on cognitive function and fatigue during extended multi-tasking. Hum Psychopharmacol 2010 Aug;25(6):448-61. https://www.ncbi.nlm.nih.gov/pubmed/20737518, abgerufen am: 04.09.2018.
Head, K.A. et al. (2009): Nutrients and Botanicals for Treatment of Stress: Adrenal Fatigue, Neurotransmitter Imbalance, Anxiety, and Restless Sleep. Altern Med Rev 2009;14(2):114-40. https://pubmed.ncbi.nlm.nih.gov/19594222/, abgerufen am: 09.08.2022.
Hidese, S. et al. (2017): Effects of chronic l-theanine administration in patients with major depressive disorder: an open-label study. Acta Neuropsychiatr 2017 Apr;29(2):72-79. https://www.ncbi.nlm.nih.gov/pubmed/27396868, abgerufen am: 10.10.2018.
Higashiyama, A. et al (2011): Effects of l-theanine on attention and reaction time response. Journal of Functional Foods 2011;3(3):171-8. https://www.sciencedirect.com/science/article/pii/S1756464611000351?via%3Dihub, abgerufen am: 07.09.2018.
Hinz, M. et al. (2012): 5-HTP efficacy and contraindications [retracted in: Neuropsychiatr Dis Treat. 2021 Mar 03;17:731]. Neuropsychiatr Dis Treat 2012 ;8:323-8. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3415362/, abgerufen am: 10.08.2022.
Hisatomi, A. et al. (1997): Elevated L-kynurenine level and its normalization by prednisolone in a patient with eosinophilia-myalgia syndrome. Fukuoka Igaku Zasshi 1997 Jan;88(1):11-7. https://pubmed.ncbi.nlm.nih.gov/9037890/, abgerufen am: 10.08.2022.
Hormonlabor Magdeburg MVZ Medizinisches Labor Prof. Schenk / Dr. Ansorge und Kollegen (2021): Dexamethason - CRH - Test (kombiniert). http://www.schenk-ansorge.de/hormonlabor/content/284/dexamethason-crh-test-kombiniert, abgerufen am: 09.08.2022.
Imura, H. et al. (1973): Effect of 5-Hydroxytryptophan (5-HTP) on growth hormone and atch release in man. Journal of Clinical Endocrinology & Metabolism 1973 Jan 1;36(1):204–6. https://academic.oup.com/jcem/article-abstract/36/1/204/2686037?redirectedFrom=fulltext&login=true, abgerufen am: 09.08.2022.
Ishaque, S. et al. (2012): Rhodiola Rosea for Physical and Mental Fatigue: A Systematic Review. BMC Complement Altern Med. 2012 May 29;12:70. https://pubmed.ncbi.nlm.nih.gov/22643043/, abgerufen am: 31.05.2021.
Ising, M. (2011): Stresshormonregulation und Depressionsrisiko – Perspektiven für die antidepressive Behandlung. Max-Planck-Gesellschaft 2011. https://www.mpg.de/4752810/Antidepressive_Behandlung, abgerufen am: 10.08.2022.
Jaroenporn, S. et al. (2008): Effects of Pantothenic Acid Supplementation on Adrenal Steroid Secretion from Male Rats. Biol Pharm Bull 2008;31(6):1205-8. https://www.jstage.jst.go.jp/article/bpb/31/6/31_6_1205/_pdf/-char/en, abgerufen am: 03.09.2018.
Jørgensen, H.S. (2007): Studies on the neuroendocrine role of serotonin. Dan Med Bull 2007; 54(4):266–88. https://www.ncbi.nlm.nih.gov/pubmed/18208678, abgerufen am: 06.09.2018.
Kanchanatawan, B. et al. (2017): Physio-somatic symptoms in schizophrenia: association with depression, anxiety, neurocognitive deficits and the tryptophan catabolite pathway. Metab Brain Dis 2017 Aug;32(4):1003-1016. https://pubmed.ncbi.nlm.nih.gov/28258445/, abgerufen am: 23.06.2021.
Kanchanatawan, B. et al (2018): In Schizophrenia, Depression, Anxiety, and Physiosomatic Symptoms Are Strongly Related to Psychotic Symptoms and Excitation, Impairments in Episodic Memory, and Increased Production of Neurotoxic Tryptophan Catabolites: a Multivariate and Machine Learning Study. Neurotox Res 2018 Apr;33(3):641-655. https://pubmed.ncbi.nlm.nih.gov/29380275/, abgerufen am: 23.06.2021.
Kent, C. & Coupland, R. E. (1984): On the uptake and storage of 5-hydroxytryptamine, 5-hydroxytryptophan and catecholamines by adrenal chromaffin cells and nerve endings. Cell Tissue Res 1984;236(1):189-95. https://pubmed.ncbi.nlm.nih.gov/6608993/, abgerufen am: 10.08.2022.
Jezova, M. et al. (2003): Angiotensin II AT(1) and AT(2) receptors contribute to maintain basal adrenomedullary norepinephrine synthesis and tyrosine hydroxylase transcription. Endocrinology 2003 May;144(5):2092-101. https://pubmed.ncbi.nlm.nih.gov/12697718/, abgerufen am: 09.08.2022.
Kaviani, M. et al. (2020): Effects of vitamin D supplementation on depression and some involved neurotransmitters. Journal of Affective Disorders 2020 May 15;269:28-35. https://www.sciencedirect.com/science/article/abs/pii/S0165032719333713?via%3Dihub, abgerufen am: 10.08.2022.
Keenan, K. et al. (2014): Association between fatty acid supplementation and prenatal stress in African Americans: a randomized controlled trial. Obstet Gynecol 2014 Dec;124(6):1080-7. https://www.ncbi.nlm.nih.gov/pubmed/25415158, abgerufen am 06.09.2018.
Kim, Y.K. et al. (2009): Cytokine changes and tryptophan metabolites in medication-naïve and medication-free schizophrenic patients. Neuropsychobiology 2009;59(2):123-9. https://pubmed.ncbi.nlm.nih.gov/19390223/, abgerufen am: 16.06.2021.
Kimura, K. et al. (2007): L-Theanine reduces psychological and physiological stress responses. Biol Psychol 2007 Jan;74(1):39-45. https://www.ncbi.nlm.nih.gov/pubmed/16930802, abgerufen am: 07.09.2018.
Klarskov, K. et al. (1999): Eosinophilia-myalgia syndrome case-associated contaminants in commercially available 5-hydroxytryptophan. Adv Exp Med Biol 1999;467:461-8. https://pubmed.ncbi.nlm.nih.gov/10721089/, abgerufen am: 09.08.2022.
Kraus, A. U. et al. (2020): Monocytic Cytokines in Autoimmune Polyglandular Syndrome Type 2 Are Modulated by Vitamin D and HLA-DQ. Front Immunol 2020;11:583709. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7750404/, abgerufen am: 10.08.2022.
Lang, R. E. et al. (1982): Evidence against co-storage of enkephalins with noradrenaline in bovine adrenal medullary granules. Eur J Pharmacol 1982 Dec 17;86(1):117-20. https://pubmed.ncbi.nlm.nih.gov/7160428/, abgerufen am: 10.08.2022.
Lanser, L. et al. (2020): Inflammation-Induced Tryptophan Breakdown is Related With Anemia, Fatigue, and Depression in Cancer. Front Immunol 2020 Feb 21;11:249. https://pubmed.ncbi.nlm.nih.gov/32153576/, abgerufen am: 23.06.2021.
Leahy, L. G.(2021): Vitamin B Supplementation: What's the Right Choice for Your Patients? Journal of Psychosocial Nursing and Mental Health Services;55(7). https://journals.healio.com/doi/abs/10.3928/02793695-20170619-02, abgerufen am: 09.08.2022.
Li Kam Wa, T.C. et al. (1993): A comparison of the renal and neuroendocrine effects of two 5-hydroxytryptamine renal prodrugs in normal man. Clin Sci (Lond) 1993 Nov;85(5):607-14. https://pubmed.ncbi.nlm.nih.gov/8287650/, abgerufen am: 28.06.2021.
Li, T. (2021): Efficacy of intravenous vitamin C intervention for septic patients: A systematic review and meta-analysis based on randomized controlled trials. Am J Emerg Med 2021 Dec;50:242-50. https://pubmed.ncbi.nlm.nih.gov/34416515/, abgerufen am: 10.08.2022.
Lieberman, H. R. et al. (2015): The catecholamine neurotransmitter precursor tyrosine increases anger during exposure to severe psychological stress. Psychopharmacology (Berl) 2015;232(5):943-51. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4325185/, abgerufen am: 10.08.2022.
Lopez-Duran, N. L. et al. (2009): Hypothalamic-pituitary-adrenal axis dysregulation in depressed children and adolescents: a meta-analysis. Psychoneuroendocrinology 2009 Oct;34(9):1272-83. https://pubmed.ncbi.nlm.nih.gov/19406581/, abgerufen am: 09.08.2022.
Ma, X. et al. (2018): Activation of GABAA Receptors in Colon Epithelium Exacerbates Acute Colitis. Front Immunol 2018 May 7;9:987. https://pubmed.ncbi.nlm.nih.gov/29867964/, abgerufen am: 23.06.2021.
Maes, M. et al. (1990): The relationships between the cortisol responses to dexamethasone and to L-5-HTP, and the availability of L-tryptophan in depressed females. Biological Psychiatry 1990 Mar 15;27(6). https://www.biologicalpsychiatryjournal.com/article/0006-3223(90)90527-9/fulltext#articleInformation, abgerufen am: 10.08.2022.
Maes, M. et al. (1987): The cortisol responses to 5-hydroxytryptophan, orally, in depressive inpatients. Journal of Affective Disorders 1987 Jul-Aug;13(1):23-30. https://www.sciencedirect.com/science/article/abs/pii/016503278790070X, abgerufen am: 10.08.2022.
Maes, M. et al. (1995): Effects of serotonin precursors on the negative feedback effects of glucocorticoids on hypothalamic-pituitary-adrenal axis function in depression. Psychoneuroendocrinology 1995;20(2):149-167. https://www.sciencedirect.com/science/article/abs/pii/030645309400049G, abgerufen am: 10.08.2022.
Maestri, E. et al. (1988): Serotonin regulation of aldosterone secretion. Horm Metab Res 1988 Jul;20(7):457-9. https://pubmed.ncbi.nlm.nih.gov/2844641/, abgerufen am: 23.06.2021.
Maffei, M. E. (2020): 5-Hydroxytryptophan (5-HTP): Natural Occurrence, Analysis, Biosynthesis, Biotechnology, Physiology and Toxicology. Int J Mol Sci 2020 Dec 26;22(1):181. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7796270/, abgerufen am: 10.08.2022.
Marik, P. E. (2020): Vitamin C: an essential "stress hormone" during sepsis. J Thorac Dis 2020;12(1):84-8. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7024758/, abgerufen am: 10.08.2022.
Markus, C.R. & Firk, C. (2009): Differential Effects of Tri-Allelic 5-HTTLPR Polymorphisms in Healthy Subjects on Mood and Stress Performance After Tryptophan Challenge. Neuropsychopharmacology 2009 Aug 12;34:2667-74. https://www.nature.com/articles/npp200992, abgerufen am: 07.09.2018.
Martínez-Rodríguez, A. et al. (2020): Psychological and Sleep Effects of Tryptophan and Magnesium-Enriched Mediterranean Diet in Women with Fibromyalgia. Int J Environ Res Public Health 2020 Mar 26;17(7):2227. https://pubmed.ncbi.nlm.nih.gov/32224987/, abgerufen am: 23.06.2021.
Matsuoka, Y.J. et al. (2016): Change in blood levels of eicosapentaenoic acid and posttraumatic stress symptom: A secondary analysis of data from a placebo-controlled trial of omega3 supplements. J Affect Disord 2016 Nov 15;205:289-91. https://www.ncbi.nlm.nih.gov/pubmed/27552592, abgerufen am: 12.09.2018.
May, J. M. et al. (2012): Mechanisms of ascorbic acid stimulation of norepinephrine synthesis in neuronal cells. Biochem Biophys Res Commun 2012;426(1):148-52. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3449284/, abgerufen am: 10.08.2022.
McCabe, D. et al. (2017): The impact of essential fatty acid, B vitamins, vitamin C, magnesium and zinc supplementation on stress levels in women: a systematic review. JBI Database System Rev Implement Rep 2017 Feb;15(2):402-453. https://pubmed.ncbi.nlm.nih.gov/28178022/, abgerufen am: 09.08.2022.
Meltzer, H. Y. et al. (1984): Effect of 5-Hydroxytryptophan on Serum Cortisol Levels in Major Affective Disorders: I. Enhanced Response in Depression and Mania. Arch Gen Psychiatry 1984;41(4):366–74. https://jamanetwork.com/journals/jamapsychiatry/article-abstract/493312, abgerufen am: 09.08.2022.
Meltzer, H. Y. et al. (1984): Effect of 5-Hydroxytryptophan on Serum Cortisol Levels in Major Affective Disorders: III. Effect of Antidepressants and Lithium Carbonate. Arch Gen Psychiatry 1984;41(4):391–7. https://jamanetwork.com/journals/jamapsychiatry/article-abstract/493314, abgerufen am: 09.08.2022.
Menon, V. et al. (2020): Vitamin D and Depression: A Critical Appraisal of the Evidence and Future Directions. Indian J Psychol Med 2020 Jan 6;42(1):11-21. https://pubmed.ncbi.nlm.nih.gov/31997861/, abgerufen am: 23.06.2021.
Morris, G. et al. (2016): The Many Neuroprogressive Actions of Tryptophan Catabolites (TRYCATs) that may be Associated with the Pathophysiology of Neuro-Immune Disorders. Curr Pharm Des 2016;22(8):963-77. https://pubmed.ncbi.nlm.nih.gov/26667000/, abgerufen am: 16.06.2021.
Mousa, A. et al. (2018): Vitamin D and symptoms of depression in overweight or obese adults: A cross-sectional study and randomized placebo-controlled trial. J Steroid Biochem Mol Biol 2018 Mar;177:200-208. https://pubmed.ncbi.nlm.nih.gov/28803880/, abgerufen am: 23.06.2021.
Murck, H. (2002): Magnesium and affective disorders. Nutr Neurosci 2002 Dec;5:375–89. https://www.ncbi.nlm.nih.gov/pubmed/12509067, abgerufen am: 06.09.2018.
Murthi, P. et al. (2017): Maternal 25-hydroxyvitamin D is inversely correlated with foetal serotonin. Clin Endocrinol (Oxf) 2017 Mar;86(3):401-409. https://pubmed.ncbi.nlm.nih.gov/27862146/, abgerufen am: 23.06.2021.
Muscogiuri, G. et al. (2015): Focus on vitamin D and the adrenal gland. Horm Metab Res 2015 Apr;47(4):239-46. https://pubmed.ncbi.nlm.nih.gov/25723858/, abgerufen am: 16.06.2021.
Muscogiuri, G. et al. (2014): Mechanisms in endocrinology: vitamin D as a potential contributor in endocrine health and disease. Eur J Endocrinol 2014 Sep;171(3):R101-10. pubmed.ncbi.nlm.nih.gov/24872497/, abgerufen am: 09.08.2022.
Muscogiuri, G. et al. Mechanisms in endocrinology: vitamin D as a potential contributor in endocrine health and disease. Eur J Endocrinol. 2014 Sep;171(3):R101-10. pubmed.ncbi.nlm.nih.gov/24872497/
Neeck, G. & Crofford, L. J. (2000): Neuroendocrine perturbations in fibromyalgia and chronic fatigue syndrome. Rheum Dis Clin North Am 2000 Nov;26(4):989-1002. https://pubmed.ncbi.nlm.nih.gov/11084955/, abgerufen am: 09.08.2022.
Nicolaides, N.C. et al. (2017): Adrenal Insufficiency. Endotext [Internet] 2000-. 2017 Oct 14. https://www.ncbi.nlm.nih.gov/books/NBK279083/, abgerufen am: 31.08.2018.
Niu, C.S. et al. (2014): Antihyperglycemic action of rhodiola-aqeous extract in type1-like diabetic rats. BMC Complement Altern Med 2014 Jan 13;14:20. https://pubmed.ncbi.nlm.nih.gov/24417880/, abgerufen am: 16.06.2021.
Omidian, M. et al. (2019): Effects of vitamin D supplementation on depressive symptoms in type 2 diabetes mellitus patients: Randomized placebo-controlled double-blind clinical trial. Diabetes Metab Syndr 2019 Jul-Aug;13(4):2375-80. https://pubmed.ncbi.nlm.nih.gov/31405646/, abgerufen am: 23.06.2021.
Overman, C. et al. (2012): Fatigue in patients with systemic lupus erythematosus: the role of dehydroepiandrosterone sulphate. Lupus 2012;21(14):1515-21. https://journals.sagepub.com/doi/abs/10.1177/0961203312459105, abgerufen am: 09.8.2022.
Panossian, A. et al. (2010): Rosenroot (Rhodiola Rosea): Traditional Use, Chemical Composition, Pharmacology and Clinical Efficacy. Phytomedicine. 2010 Jun;17(7):481-93. https://pubmed.ncbi.nlm.nih.gov/20378318/, abgerufen am: 31.05.2021.
Panossian, A. & Wikman, G. (2009): Evidence-based efficacy of adaptogens in fatigue, and molecular mechanisms related to their stress-protective activity. Curr Clin Pharmacol 2009 Sep;4(3):198-219. https://pubmed.ncbi.nlm.nih.gov/19500070/, abgerufen am: 09.08.2022.
Patak, P. et al. (2004): Vitamin C is an important cofactor for both adrenal cortex and adrenal medulla. Endocr Res 2004 Nov;30(4):871-5. https://pubmed.ncbi.nlm.nih.gov/15666839/, abgerufen am: 09.08.2022.
Patrick, R.P. & Ames, B.N. (2014): Vitamin D hormone regulates serotonin synthesis. Part 1: relevance for autism. FASEB J 2014 Jun;28(6):2398-413. https://pubmed.ncbi.nlm.nih.gov/24558199/, abgerufen am: 16.06.2021.
Peel, J. S. et al. (2021): The Effect of Dietary Supplements on Endurance Exercise Performance and Core Temperature in Hot Environments: A Meta-analysis and Meta-regression. Sports Med 2021;51(11):2351-71. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8514372/, abgerufen am: 10.08.2022.
Penna-Martinez, M. (2018): High-dose vitamin D in Addison's disease regulates T-cells and monocytes: A pilot trial Nutrition. 2018 May;49:66-73. https://pubmed.ncbi.nlm.nih.gov/29522979/, abgerufen am: 10.08.2022.
Penna-Martinez, M. et al. (2021): Vitamin D status and pathway genes in five European autoimmune Addison's disease cohorts. Eur J Endocrinol 2021 Mar;184(3):373-81. https://pubmed.ncbi.nlm.nih.gov/33444227/, abgerufen am: 10.08.2022.
Peters, E.M. et al. (2001): Vitamin C supplementation attenuates the increases in circulating cortisol, adrenaline and anti-inflammatory polypeptides following ultramarathon running. Int J Sports Med 2001 Oct;22(7):537-43. https://www.ncbi.nlm.nih.gov/pubmed/11590482, abgerufen am: 05.09.2018.
Porter, R J. et al. (2004): Corticosteroid-serotonin interactions in depression: a review of the human evidence. Psychopharmacology (Berl) 2004 Apr;173(1-2):1-17. https://www.ncbi.nlm.nih.gov/pubmed/15007595, abgerufen am: 07.09.2018.
Pu, W.-l. et al. (2020): Anti-inflammatory effects of Rhodiola rosea L.: A review. Biomedicine & Pharmacotherapy 2020;121:109552. https://www.sciencedirect.com/science/article/pii/S0753332219329671?via%3Dihub, abgerufen am: 28.06.2021.
Putzu, A. et al. (2019): The Effect of Vitamin C on Clinical Outcome in Critically Ill Patients: A Systematic Review With Meta-Analysis of Randomized Controlled Trials. Crit Care Med 2019 Jun;47(6):774-83. https://pubmed.ncbi.nlm.nih.gov/30839358/, abgerufen am: 10.08.2022.
Quinkler, M. et al. (2013): Adrenal Cortical Insufficiency—a Life Threatening Illness With Multiple Etiologies. Dtsch Arztebl Int 2013;110(51-52):882-8. https://www.endokrinologie.net/files/download/nn_aerzteblatt_2013_0882.pdf, abgerufen am: 10.08.2022.
Rasmussen, D. D. et al. (1983): Effects of tyrosine and tryptophan ingestion on plasma catecholamine and 3,4-dihydroxyphenylacetic acid concentrations. J Clin Endocrinol Metab 1983 Oct;57(4):760-3. https://pubmed.ncbi.nlm.nih.gov/6885965/, abgerufen am: 10.08.2022.
Rolf, L. et al (2018): Stress-Axis Regulation by Vitamin D3 in Multiple Sclerosis. Front Neurol 2018 Apr 26;9:263. https://pubmed.ncbi.nlm.nih.gov/29755397/, abgerufen am: 23.06.2021.
Römer, G. et al. (2020): 5-Hydroxytryptophan. DocCheck Flexikon 2020 Jan 6. https://flexikon.doccheck.com/de/5-Hydroxytryptophan, abgerufen am: 09.08.2022.
Rosengrave, P. et al. (2022): Intravenous vitamin C administration to patients with septic shock: a pilot randomised controlled trial. Crit Care 2022 Jan 25;26(1):26. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8786621/, abgerufen am: 10.08.2022.
Rosse, R.B. et al. (1992): Effect of a low-tryptophan diet as an adjuvant to conventional neuroleptic therapy in schizophrenia. Clin Neuropharmacol 1992 Apr;15(2):129-41. https://pubmed.ncbi.nlm.nih.gov/1350512/, abgerufen am: 16.06.2021.
Salman-Monte, T. C. (2016): Prevalence and predictors of vitamin D insufficiency in supplemented and non-supplemented women with systemic lupus erythematosus in the Mediterranean region. Rheumatol Int. 2016 Jul;36(7):975-85. https://pubmed.ncbi.nlm.nih.gov/27233506/, abgerufen am: 09.08.2022.
Santoro, D. et al. (2015): Interplay of vitamin D, erythropoiesis, and the renin-angiotensin system. Biomed Res Int 2015;2015:145828. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4427087/, abgerufen am: 28.06.2021.
Sawazaki, S. et al. (1999): The effect of docosahexaenoic acid on plasma catecholamine concentrations and glucose tolerance during long-lasting psychological stress: a double-blind placebo-controlled study. J Nutr Sci Vitaminol (Tokyo) 1999 Oct;45(5):655-65. https://www.ncbi.nlm.nih.gov/pubmed/10683816, abgerufen am: 11.09.2018.
Schüle, C. et al. (2014): The role of allopregnanolone in depression and anxiety. Prog Neurobiol 2014 Feb;113:79-87. https://pubmed.ncbi.nlm.nih.gov/24215796/, abgerufen am 16.06.2021.
Sedaghat, K. et al. (2019): Mesolimbic dopamine system and its modulation by vitamin D in a chronic mild stress model of depression in the rat. Behav Brain Res 2019 Jan 1;356:156-169. https://pubmed.ncbi.nlm.nih.gov/30144460/, abgerufen am: 23.06.2021.
Seelig, M. S. (1998): Consequences of magnesium deficiency on the enhancement of stress reactions; preventive and therapeutic implications (a review). J Am Coll Nutr 1994 Oct;13(5):429-46. https://www.ncbi.nlm.nih.gov/pubmed/7836621, abgerufen am: 06.09.2018.
Shenker, Y. et al. (1985): Peripheral serotonin2 receptor blockade does not inhibit 5-hydroxytryptophan-induced aldosterone stimulation. J Clin Endocrinol Metab 1985 Dec;61(6):1201-4. https://pubmed.ncbi.nlm.nih.gov/2932460/, abgerufen am: 10.08.2022.
Sher, L. (2006): Combined dexamethasone suppression-corticotropin-releasing hormone stimulation test in studies of depression, alcoholism, and suicidal behavior. ScientificWorldJournal 2006 Oct 31;6:1398-404. https://pubmed.ncbi.nlm.nih.gov/17086345/, abgerufen am: 09.08.2022.
Silbernagel, S. et al. (2003): Taschenatlas der Physiologie. Thieme, Stuttgart.
Silver, R. M. et al. (1990): Scleroderma, fasciitis, and eosinophilia associated with the ingestion of tryptophan. N Engl J Med 1990 Mar 29;322(13):874-81. https://pubmed.ncbi.nlm.nih.gov/1690352/, abgerufen am: 09.08.2022.
Sirivichayakul, S. et al. (2019): A New Schizophrenia Model: Immune Activation is Associated with the Induction of Different Neurotoxic Products which Together Determine Memory Impairments and Schizophrenia Symptom Dimensions. CNS Neurol Disord Drug Targets 2019;18(2):124-140. https://pubmed.ncbi.nlm.nih.gov/30451122/, abgerufen am: 23.06.2021.
Sobrinho, L.G. (2003): Prolactin, psychological stress and environment in humans: adaptation and maladaptation. Pituitary 2003;6(1):35-9. https://www.ncbi.nlm.nih.gov/pubmed/14674722, abgerufen am: 06.09.2018.
Stough, C. et al. (2011). The effect of 90 day administration of a high dose vitamin B-complex on work stress. Hum Psychopharmacol 2011 Oct;26(7):470-6. https://www.ncbi.nlm.nih.gov/pubmed/21905094, abgerufen am: 04.09.2018.
Stough, C. et al. (2014): Reducing occupational stress with a B-vitamin focussed intervention: a randomized clinical trial: study protocol. Nutr J 2014; 13:22. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4290459/, abgerufen am: 03.09.2018.
Tarleton, E.K. et al. (2017): Role of magnesium supplementation in the treatment of depression: A randomized clinical trial. PLOS ONE 2017;12(6):e0180067. https://journals.plos.org/plosone/article?id=10.1371/journal.pone.0180067, abgerufen am: 22.10.2018.
Tirabassi, G. et al. (2017): Adrenal disorders: Is there Any role for vitamin D? Rev Endocr Metab Disord 2017 Sep;18(3):355-362. https://pubmed.ncbi.nlm.nih.gov/27761790/, abgerufen am: 16.06.2021.
Tardy, A. L. et al. (2020): Vitamins and Minerals for Energy, Fatigue and Cognition: A Narrative Review of the Biochemical and Clinical Evidence. Nutrients 2020 Jan 16;12(1):228. https://pubmed.ncbi.nlm.nih.gov/31963141/, abgerufen am: 10.08.2022.
Tremblay, S. (2011): 5-HTP & Cortisol. Healthfully 2011 Oct 19. https://healthfully.com/548278-5-htp-cortisol.html, abgerufen am: 09.08.2022.
Trulson, M.E. & Ulissey, M.J. (1987): Low doses of L-tryptophan are lethal in rats with adrenal insufficiency. Life Sci 1987 Jul 20;41(3):349-53. https://pubmed.ncbi.nlm.nih.gov/3079519/, abgerufen am: 23.06.2021.
Universitätsspital-Zürich: Nebennierenunterfunktion – Morbus Addison. https://www.usz.ch/krankheit/nebennierenunterfunktion/#:~:text=Die%20sekundäre%20Nebennierenunterfunktion%20entsteht%20durch,von%20einer%20Millionen%20Menschen%20auf, abgerufen am 31.01.2023
Vaziri, F. et al. (2016): A randomized controlled trial of vitamin D supplementation on perinatal depression: in Iranian pregnant mothers. BMC Pregnancy Childbirth 2016 Aug 20;16:239. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4992225/, abgerufen am: 28.06.2021.
Velickovix, D. et al. (2014). The study of vitamins B1, B6, and B12 effects on adrenal cortex adaption by monitoring some enzyme systems in rats trained by swimming. Acta Medica Medianae 2014;53(2):33. http://scindeks-clanci.ceon.rs/data/pdf/0365-4478/2014/0365-44781402033V.pdf, abgerufen am: 04.09.2018.
Wang, Y. et al. (2013): Effects of vitamin C and vitamin D administration on mood and distress in acutely hospitalized patients. Am J Clin Nutr 2013;98(3):705-11. https://www.ncbi.nlm.nih.gov/pubmed/23885048, abgerufen am: 05.09.2018.
Watts, S.W. et al. (2021): Serotonin and blood pressure regulation. Pharmacol Rev 2012;64(2):359-388. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3310484/, abgerufen am: 28.06.2021.
White, D.J. et al. (2016): Anti-Stress, Behavioural and Magnetoencephalography Effects of an l-Theanine-Based Nutrient Drink: A Randomised, Double-Blind, Placebo-Controlled, Crossover Trial. Nutrients 2016;8(1):53. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4728665/, abgerufen am: 07.09.2018.
Whyte, K.F. et al. (1987): Adrenergic control of plasma magnesium in man. Clin Sci (Lond) 1987 Jan;72(1):135–8. https://www.ncbi.nlm.nih.gov/pubmed/3542342, abgerufen am: 06.09.2018.
Willenberg, H. et al. (2020): Nebennierenhormonmangel - "Nebenniereninsuffizienz". Deutsche Gesellschaft für Endokrinologie 2020. https://www.endokrinologie.net/krankheiten-nebenniereninsuffizienz.php, abgerufen am: 10.08.2022.
Wilson, J.L. (2014): Clinical perspective on stress, cortisol and adrenal fatigue. Advances in Integrative Medicine 2014;1(2):93-96. https://www.aimedjournal.com/article/S2212-9626(14)00005-4/pdf, abgerufen am: 03.09.2018.
Xu, W. et al. (2013): Two potent cytochrome P450 2D6 inhibitors found in Rhodiola rosea. Pharmazie. 2013 Dec;68(12):974-6. https://pubmed.ncbi.nlm.nih.gov/24400445/, abgerufen am: 16.06.2021.
Yamamoto, T. et al. (2012): Essential role of excessive tryptophan and its neurometabolites in fatigue. Can J Neurol Sci 2012 Jan;39(1):40-7. https://pubmed.ncbi.nlm.nih.gov/22384494/, abgerufen am: 16.06.2021.
Yamamoto, T. et al. (2012): Essential role of excessive tryptophan and its neurometabolites in fatigue. Can J Neurol Sci 2012 Jan;39(1):40-7. https://pubmed.ncbi.nlm.nih.gov/22384494/, abgerufen am: 09.08.2022.
Yamamoto, T. (2014): History of Stress-related Health Changes: A Cue to Pursue a Diagnosis of Latent Primary Adrenal Insufficiency. Internal medicine 2014;53:183-8. https://www.researchgate.net/publication/260090844_History_of_Stress-related_Health_Changes_A_Cue_to_Pursue_a_Diagnosis_of_Latent_Primary_Adrenal_Insufficiency/citation/download, abgerufen am: 10.08.2022.
Yamashita, M. & Yamamoto, T. (2014): Tryptophan and kynurenic Acid may produce an amplified effect in central fatigue induced by chronic sleep disorder. Int J Tryptophan Res 2014 May 14;7:9-14. https://pubmed.ncbi.nlm.nih.gov/24899814/, abgerufen am 09.08.2022.
Yamashita, M. (2020): Potential Role of Neuroactive Tryptophan Metabolites in Central Fatigue: Establishment of the Fatigue Circuit. Int J Tryptophan Res 2020;13:1178646920936279. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7325545/, abgerufen am: 28.06.2021.
Yamashita M. (2020): Potential Role of Neuroactive Tryptophan Metabolites in Central Fatigue: Establishment of the Fatigue Circuit. Int J Tryptophan Res 2020 Jun 29;13:1178646920936279. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7325545/, abgerufen am: 10.08.2022.
Yosaee, S. et al. (2020): Effects of zinc, vitamin D, and their co-supplementation on mood, serum cortisol, and brain-derived neurotrophic factor in patients with obesity and mild to moderate depressive symptoms: A phase II, 12-wk, 2 × 2 factorial design, double-blind, randomized, placebo-controlled trial. Nutrition 2020 Mar;71:110601. https://pubmed.ncbi.nlm.nih.gov/31837640/, abgerufen am: 23.06.2021.
Yoto, A. et al. (2012): Oral intake of γ-aminobutyric acid affects mood and activities of central nervous system during stressed condition induced by mental tasks. Amino Acids 2012;43(3):1331-7. https://www.ncbi.nlm.nih.gov/pubmed/22203366, abgerufen am: 07.09.2018.
Yoto, A. et al. (2012): Effects of L-theanine or caffeine intake on changes in blood pressure under physical and psychological stresses. J Physiol Anthropol 2012 Sep; 31(1): 28. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3518171, abgerufen am: 10.10.2018.
Younes, N. et al. (2021): Bourdeau I, Lacroix A. Latent Adrenal Insufficiency: From Concept to Diagnosis. Front Endocrinol (Lausanne) 2021 Aug 27;12:720769. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8429826/, abgerufen am: 10.08.2022.
Young, L.M. et al. (2019): A Systematic Review and Meta-Analysis of B Vitamin Supplementation on Depressive Symptoms, Anxiety, and Stress: Effects on Healthy and 'At-Risk' Individuals. Nutrients 2019 Sep 16;11(9):2232. https://pubmed.ncbi.nlm.nih.gov/31527485/, abgerufen am: 23.06.2021.
Zawadzka, K. et al. (2021): Vitamin D status and its associations with clinical and laboratory parameters in patients with Addison's disease. Folia Med Cracov 2021;61(2):65-78. https://pubmed.ncbi.nlm.nih.gov/34510165/, abgerufen am: 10.08.2022.
Zhang, C. X. et al. (2020): Immunometabolism in the pathogenesis of systemic lupus erythematosus. J Transl Autoimmun 2020;3:100046. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7388408/, abgerufen am: 10.08.2022.
Zhang, X. et al. (2018): Stress-Induced Functional Alterations in Amygdala: Implications for Neuropsychiatric Diseases. Front Neurosci 2018;12:367. https://www.ncbi.nlm.nih.gov/pmc/articles/PMC5987037/, abgerufen am: 07.09.2018.
Zhou, Y. H. et al. (2019): Tryptophan Metabolism Activates Aryl Hydrocarbon Receptor-Mediated Pathway To Promote HIV-1 Infection and Reactivation. mBio 2019 Dec 17;10(6):e02591-19. https://pubmed.ncbi.nlm.nih.gov/31848275/, abgerufen am: 10.08.2022.
Zofková, I. & Kancheva, R.L. (1994): Lack of stimulatory effect of 1,25(OH)2 vitamin D3 on beta-endorphin and cortisol secretion. J Endocrinol Invest 1994 Oct;17(9):693-5. https://pubmed.ncbi.nlm.nih.gov/7868812/, abgerufen am: 28.06.2021.